题目内容
已知:Na2CO3+CaCl2═ CaCO3↓+2NaCl
CaCO3↓+2NaCl
请根据下图所示的实验过程和有关数据,回答问题:

⑴ 恰好完全反应时生成的CaCO3沉淀质量为多少克?
⑵原混合物样品中NaCl的质量为多少克?(要求写 出计算过程)
出计算过程)
解:⑴碳酸钙沉淀的质量为:
22.3g+100.0g+80g﹣192.3g=10.0g ………………………1分
⑵设混合物中碳酸钠的质量为x ………………………1分
Na2CO3+CaCl2═CaCO3↓+2NaCl
106 100
x 10.0g
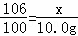 解得:x=10.6g ………………………2分
解得:x=10.6g ………………………2分
氯化钠质量:22.3g﹣10.6g=11.7g ………………………1分
答:样品中中氯化钠的质量为11.7g
(设答完 整给1分)
整给1分)

练习册系列答案
相关题目
 已知CaCl2+Na2CO3=CaCO3↓+2NaCl.将15g CaCl2溶液逐滴加入到20g Na2CO3溶液中,并测得生成沉淀的质量与滴入CaCl2溶液的质量关系如图所示.若将反应后的物质过滤,蒸干滤液后得到固体的质量是多少.
已知CaCl2+Na2CO3=CaCO3↓+2NaCl.将15g CaCl2溶液逐滴加入到20g Na2CO3溶液中,并测得生成沉淀的质量与滴入CaCl2溶液的质量关系如图所示.若将反应后的物质过滤,蒸干滤液后得到固体的质量是多少.