题目内容
(5分)过氧化钠(Na2O2)与水发生反应,生成对应的碱和氧气,化学方程式为:2Na2O2+2H2O=4NaOH+O2↑。现将78 g过氧化钠放入338 g水中,充分反应。试计算:
(1)生成的氧气在标准状况的体积是多少?(已知标准状况下氧气的密度是1.43g/L)
(2)所得溶液中溶质质量分数是多少?
解:设生成O2和NaOH的质量分别为x和y
2Na2O2 + 2H2O =" 4NaOH " + O2↑
156 160 32
78g y x

x="16" g
y="80" g
故O2在标准状况下的体积为: =" 11.2" L
=" 11.2" L
NaOH溶液中NaOH的质量分数为: ×100% =20%解析:
×100% =20%解析:
略
2Na2O2 + 2H2O =" 4NaOH " + O2↑
156 160 32
78g y x

x="16" g
y="80" g
故O2在标准状况下的体积为:
 =" 11.2" L
=" 11.2" LNaOH溶液中NaOH的质量分数为:
 ×100% =20%解析:
×100% =20%解析:略

练习册系列答案
 星级口算天天练系列答案
星级口算天天练系列答案
相关题目
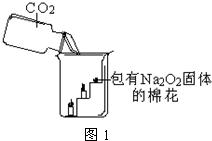


 23、呼吸面具和潜水艇中可用过氧化钠(Na2O2)作为供氧剂.下面是兴趣小组同学围绕过氧化钠进行的一系列探究,请你参与到其中.
23、呼吸面具和潜水艇中可用过氧化钠(Na2O2)作为供氧剂.下面是兴趣小组同学围绕过氧化钠进行的一系列探究,请你参与到其中.
