题目内容
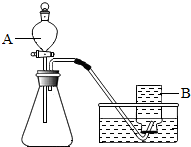
某兴趣小组根据实验室提供的仪器和药品进行了氧气的制备实验.(1)甲同学选用如右图所示的装置制取氧气.
①写出仪器A的名称:______.
②甲同学应选取的试剂是MnO2和______(填化学式),MnO2固体在该反应中起______作用.
③除用排水法外,甲同学还可选择______法收集氧气.
(2)乙同学称取一定质量KMnO4放在大试管中,将温度控制在250℃加热制取O2,该反
应的反应表达式为______ K2MnO4+MnO2+O2↑

【答案】分析:(1)根据制取氧气的装置图中发生装置的适用范围及对氧气制取反应原理、密度与溶解性,判断利用该装置的制取氧气所选用的药品、收集氧气可采取的方法;
(2)默写出高锰酸钾分解制取氧气的化学方程式;
【提出猜想】根据变化前后元素种类不变,利用锰酸钾、二氧化锰的组成特点,对所作的猜想进行评价;
【实验验证】①二氧化锰加热前后质量未变,说明二氧化锰在加热时未发生分解,也就不可能产生氧气;
②可利用氧气能使带火星木条复燃的特点,利用带火星木条进行检验分解出氧气而不必进行质量的称量.
解答:解:(1)①仪器A为加入液体药品的分液漏斗;
②该发生装置适用于固体药品与液体常温下发生反应制取气体,即使用该装置时应加入的药品为固体二氧化锰、液体过氧化氢,其中固体二氧化锰催化过氧化氢的分解,是该反应的催化剂;
③利用氧气密度比空气大,因此还可以采取向上排空气法进行氧气的收集;
(2)高锰酸钾在加热条件下分解生成锰酸钾、二氧化锰和氧气,反应的化学方程式为2KMnO4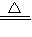 K2MnO4+MnO2+O2↑;
K2MnO4+MnO2+O2↑;
【提出猜想】对比K2MnO4和MnO2的组成,都含有氧元素,根据质量守恒定律变化前后元素种类不变,所以猜想它们受热分解出氧气;
【实验验证】①加热前后二氧化锰的质量不变,可证明加热时二氧化锰未发生反应,即未分解出氧气,此实验验证了猜想I不成立;
②如果K2MnO4分解放出O2的猜想成立,那么在加热锰酸钾时将带火星木条伸入试管,观察到木条复燃则可说明分解放出了氧气,而不必进行变化前后的质量称量.
故答案为:
(1)①分液漏斗;②H2O2;催化;③向上排空气法;
(2)2KMnO4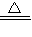 K2MnO4+MnO2+O2↑;
K2MnO4+MnO2+O2↑;
【提出猜想】K2MnO4和MnO2中都含有氧元素;
【实验验证】①Ⅰ;②将带火星的木条伸入试管,若木条复燃,则猜想Ⅱ正确
点评:熟练掌握实验室制取氧气的反应原理、发生装置、收集方法及氧气的检验等基础,结合质量守恒定律的运用对猜想进行解释,考查实验能力.
(2)默写出高锰酸钾分解制取氧气的化学方程式;
【提出猜想】根据变化前后元素种类不变,利用锰酸钾、二氧化锰的组成特点,对所作的猜想进行评价;
【实验验证】①二氧化锰加热前后质量未变,说明二氧化锰在加热时未发生分解,也就不可能产生氧气;
②可利用氧气能使带火星木条复燃的特点,利用带火星木条进行检验分解出氧气而不必进行质量的称量.
解答:解:(1)①仪器A为加入液体药品的分液漏斗;
②该发生装置适用于固体药品与液体常温下发生反应制取气体,即使用该装置时应加入的药品为固体二氧化锰、液体过氧化氢,其中固体二氧化锰催化过氧化氢的分解,是该反应的催化剂;
③利用氧气密度比空气大,因此还可以采取向上排空气法进行氧气的收集;
(2)高锰酸钾在加热条件下分解生成锰酸钾、二氧化锰和氧气,反应的化学方程式为2KMnO4
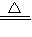 K2MnO4+MnO2+O2↑;
K2MnO4+MnO2+O2↑;【提出猜想】对比K2MnO4和MnO2的组成,都含有氧元素,根据质量守恒定律变化前后元素种类不变,所以猜想它们受热分解出氧气;
【实验验证】①加热前后二氧化锰的质量不变,可证明加热时二氧化锰未发生反应,即未分解出氧气,此实验验证了猜想I不成立;
②如果K2MnO4分解放出O2的猜想成立,那么在加热锰酸钾时将带火星木条伸入试管,观察到木条复燃则可说明分解放出了氧气,而不必进行变化前后的质量称量.
故答案为:
(1)①分液漏斗;②H2O2;催化;③向上排空气法;
(2)2KMnO4
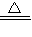 K2MnO4+MnO2+O2↑;
K2MnO4+MnO2+O2↑;【提出猜想】K2MnO4和MnO2中都含有氧元素;
【实验验证】①Ⅰ;②将带火星的木条伸入试管,若木条复燃,则猜想Ⅱ正确
点评:熟练掌握实验室制取氧气的反应原理、发生装置、收集方法及氧气的检验等基础,结合质量守恒定律的运用对猜想进行解释,考查实验能力.

练习册系列答案
 阳光考场单元测试卷系列答案
阳光考场单元测试卷系列答案 名校联盟冲刺卷系列答案
名校联盟冲刺卷系列答案 名校提分一卷通系列答案
名校提分一卷通系列答案 课程达标测试卷闯关100分系列答案
课程达标测试卷闯关100分系列答案
相关题目
 某兴趣小组根据实验室提供的仪器和药品进行了氧气的制备实验.
某兴趣小组根据实验室提供的仪器和药品进行了氧气的制备实验. 某兴趣小组根据实验室提供的仪器和药品进行了氧气的制备实验.
某兴趣小组根据实验室提供的仪器和药品进行了氧气的制备实验.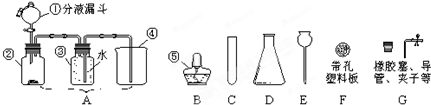
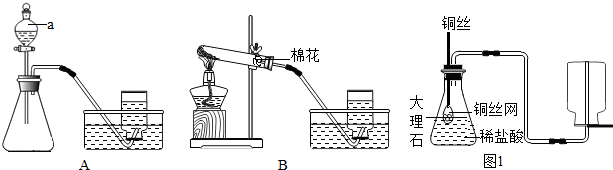
 某兴趣小组根据实验室提供的仪器和药品进行了氧气的制备实验.
某兴趣小组根据实验室提供的仪器和药品进行了氧气的制备实验.