题目内容
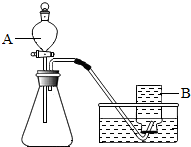 某兴趣小组根据实验室提供的仪器和药品进行了氧气的制备实验.
某兴趣小组根据实验室提供的仪器和药品进行了氧气的制备实验.(1)甲同学选用如图所示的装置制取氧气.
写出仪器B的名称:
②甲同学应选取的试剂是Mn02和
Mn02固体在该反应中起
③除用排水法外,甲同学还可选择
④实验前,甲同学先向仪器A中加入水,然后将导管放人水槽中,并打开仪器A的活塞,观察导管口是否有连续的气泡出现.该实验操作的目的是
(2)乙同学称取一定质量KMn04放在大试管中,将温度控制在250℃加热制取O2,该反
应的化学方程式为
【提出猜想】猜想l:反应生成的MnO2分解放出02;
猜想Ⅱ:反应生成的K2Mn04分解放出O2
做出上述猜想的理由是
【实验验证】同学们分为两组,分别进行以下实验:
①第一组同学取一定质量的Mn02,在250℃条件下加热一段时间,冷却后测得Mn02的质量不变.则猜想
②第二组同学取K2Mn04在250℃条件下加热,没有用测定质量的方法得出了猜想Ⅱ正确的结论.该组同学选择的实验方法是
【拓展延伸】实验发现,K2MnO4受热只能部分分解,经分析可能是生成物K2O对其分
解产生影响.请设计实验方案验证:
【实验反思】通过以上实验探究,你对“问题的发现与解决”有何认识?
分析:(1)熟悉常见仪器,了解名称;②根据反应装置和所提供药品,确定另一种药品;根据二氧化锰在反应中的表现了解作用;③根据氧气的密度和溶水性考虑收集方法;④实验前要检验装置的气密性;
(2)根据反应物、反应条件、生成物写出化学反应式;
【提出猜想】有氧气生成就要有氧元素存在;
【实验验证】要验证猜想II,可以用验证氧气的方法来确定氧气的有无,可以用带火星的木条深入收集的气体中,观察现象;
【拓展延伸】使两者形成对比,取等量的K2MnO4,其中一个加入K2O,另一个不加K2O,各自收集一瓶氧气,看所用的时间长短来确定,是否是K2O的影响;
【实验反思】总结实验的分析和解决过程,然后了解到需认真分析,并根据科学的方法去验证.
(2)根据反应物、反应条件、生成物写出化学反应式;
【提出猜想】有氧气生成就要有氧元素存在;
【实验验证】要验证猜想II,可以用验证氧气的方法来确定氧气的有无,可以用带火星的木条深入收集的气体中,观察现象;
【拓展延伸】使两者形成对比,取等量的K2MnO4,其中一个加入K2O,另一个不加K2O,各自收集一瓶氧气,看所用的时间长短来确定,是否是K2O的影响;
【实验反思】总结实验的分析和解决过程,然后了解到需认真分析,并根据科学的方法去验证.
解答:解:(1)图中B是集气瓶.
故答案为:集气瓶;
②如图装置适合固液不加热反应,我们可以用过氧化氢溶液和固体二氧化锰反应制取氧气,其中二氧化锰在反应前后性质和质量都不发生变化,所以二氧化锰起催化作用.
故答案为:H2O2、催化;
③因氧气的密度大于空气的密度,不易溶于水,所以除用排水法收集外,还可以用向上排空气法收集.
故答案为:向上排空气法;
④这种做法可以使装置内外形成压力差,看装置是否漏气.
故答案为:检验装置的气密性;
(2)加热高锰酸钾制取氧气的化学反应式是:2KMnO4
K2MnO4+MnO2+O2↑;
故答案为:2KMnO4
K2MnO4+MnO2+O2↑;
【提出猜想】K2Mn04和MnO2都是含有氧元素的化合物,所以我们可以猜想有氧气生成.
故答案为:K2Mn04和MnO2都是含有氧元素的化合物.
【实验验证】①根据质量守恒定义和冷却后测得Mn02的质量不变可知,猜想I是错误的,故答案为:I;
②我们可以用验证氧气有无的方法去判断是否有氧气的生成,如用带火星的木条,深入收集的气体中,如果木条复燃说明有氧气生成.
故答案为:检验是否有氧气生成.
【拓展延伸】我们可以用如下实验验证:取等量的固体于两支试管中,一支试管中加入氧化钾,一支试管中不加氧化钾.用同样火焰的酒精灯加热,用相同规格的集气瓶,用排水法收集气体,收集一瓶氧气,所用时间作比较,确定锰酸钾的分解是否与氧化钾有关系.
故答案为:取等量的固体于两支试管中,一支试管中加入氧化钾,一支试管中不加氧化钾.用同样火焰的酒精灯加热,用相同规格的集气瓶,用排水法收集气体,收集一瓶氧气,所用时间作比较,确定锰酸钾的分解是否与氧化钾有关系.
【实验反思】要想发现问题,必须细心认真;要想解决问题,必须认真分析问题的原因所在,并用实验去验证,故答案为:必须通过认真分析,用实验来加以证明.
故答案为:集气瓶;
②如图装置适合固液不加热反应,我们可以用过氧化氢溶液和固体二氧化锰反应制取氧气,其中二氧化锰在反应前后性质和质量都不发生变化,所以二氧化锰起催化作用.
故答案为:H2O2、催化;
③因氧气的密度大于空气的密度,不易溶于水,所以除用排水法收集外,还可以用向上排空气法收集.
故答案为:向上排空气法;
④这种做法可以使装置内外形成压力差,看装置是否漏气.
故答案为:检验装置的气密性;
(2)加热高锰酸钾制取氧气的化学反应式是:2KMnO4
| ||
故答案为:2KMnO4
| ||
【提出猜想】K2Mn04和MnO2都是含有氧元素的化合物,所以我们可以猜想有氧气生成.
故答案为:K2Mn04和MnO2都是含有氧元素的化合物.
【实验验证】①根据质量守恒定义和冷却后测得Mn02的质量不变可知,猜想I是错误的,故答案为:I;
②我们可以用验证氧气有无的方法去判断是否有氧气的生成,如用带火星的木条,深入收集的气体中,如果木条复燃说明有氧气生成.
故答案为:检验是否有氧气生成.
【拓展延伸】我们可以用如下实验验证:取等量的固体于两支试管中,一支试管中加入氧化钾,一支试管中不加氧化钾.用同样火焰的酒精灯加热,用相同规格的集气瓶,用排水法收集气体,收集一瓶氧气,所用时间作比较,确定锰酸钾的分解是否与氧化钾有关系.
故答案为:取等量的固体于两支试管中,一支试管中加入氧化钾,一支试管中不加氧化钾.用同样火焰的酒精灯加热,用相同规格的集气瓶,用排水法收集气体,收集一瓶氧气,所用时间作比较,确定锰酸钾的分解是否与氧化钾有关系.
【实验反思】要想发现问题,必须细心认真;要想解决问题,必须认真分析问题的原因所在,并用实验去验证,故答案为:必须通过认真分析,用实验来加以证明.
点评:本题考查制取氧气的实验以及相关问题,还有验证猜想的实验设计,要同学们具有综合的化学知识才可做好此题.

练习册系列答案
相关题目
 某兴趣小组根据实验室提供的仪器和药品进行了氧气的制备实验.
某兴趣小组根据实验室提供的仪器和药品进行了氧气的制备实验.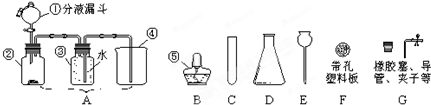
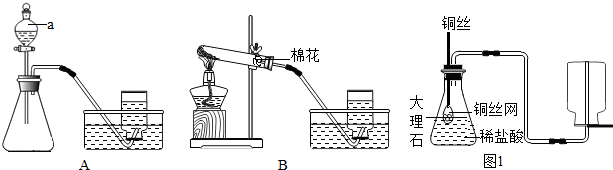
 某兴趣小组根据实验室提供的仪器和药品进行了氧气的制备实验.
某兴趣小组根据实验室提供的仪器和药品进行了氧气的制备实验.