题目内容
9.下列说法错误的是( )| A. | 垃圾是放错了地方的资源 | |
| B. | 低碳生活、节能减排,可减少温室气体排放 | |
| C. | 工业盐NaNO2有咸味,也可以用来食品调味 | |
| D. | 合理使用化肥,提高农作物产量,缓解粮食危机 |
分析 A、根据垃圾中含有大量可回收利用的资源,进行分析判断.
B、根据低碳生活、节能减排的含义进行分析判断.
C、根据NaNO2有毒进行分析判断.
D、根据化肥和农药的作用进行分析判断.
解答 解:A、垃圾中含有大量可回收利用的资源,垃圾是放错地方的资源,应分类回收利用,故选项说法正确.
B、低碳生活、节能减排,是指生活中尽量减少二氧化碳等温室气体的排放,体现低能耗、低能量、低开支,故选项说法正确.
C、NaNO2有毒,不可以用来调味,故选项说法错误.
D、合理使用化肥,提高农作物产量,缓解粮食危机,故选项说法正确.
故选:C.
点评 本题考查了化学与生产、生活联系密切的有关知识,突出了化学的实用性,平时要注意积累.

练习册系列答案
 阳光试卷单元测试卷系列答案
阳光试卷单元测试卷系列答案
相关题目
19.下列有关金属及合金的说法中正确的是( )
| A. | “真金不怕火炼”说明黄金的硬度非常大 | |
| B. | 金属活动顺序表中,银前面的金属都能置换出AgCl中的银 | |
| C. | 合金是由两种或两种以上金属熔合而成的具有金属特性的物质 | |
| D. | 在日常生活中,大量使用的常常不是纯金属,而是它们的合金 |
20.下列各组物质在水中一定能大量共存的是( )
| A. | KOH、HCl、NaHCO3 | B. | NaCl、BaCl2、K2CO3 | ||
| C. | NH4Cl、NaNO3、K2CO3 | D. | CuCl2、NaCl、NaOH |
4.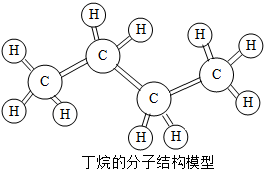 液化石油气是经加压后到钢瓶中的,瓶内压强是大气压强的7-8倍,液化石油气的主要成分是丙烷、丁烷、丙烯和丁烯等.下列有关与丁烷的叙述正确的是( )
液化石油气是经加压后到钢瓶中的,瓶内压强是大气压强的7-8倍,液化石油气的主要成分是丙烷、丁烷、丙烯和丁烯等.下列有关与丁烷的叙述正确的是( )
 液化石油气是经加压后到钢瓶中的,瓶内压强是大气压强的7-8倍,液化石油气的主要成分是丙烷、丁烷、丙烯和丁烯等.下列有关与丁烷的叙述正确的是( )
液化石油气是经加压后到钢瓶中的,瓶内压强是大气压强的7-8倍,液化石油气的主要成分是丙烷、丁烷、丙烯和丁烯等.下列有关与丁烷的叙述正确的是( )| A. | 丁烷中碳、氢元素的个数比为2:5 | B. | 丁烷分子中氢元素的质量分数最大 | ||
| C. | 丁烷是由碳、氢原子构成的 | D. | 在通常状况下,丁烷是气体 |
14.下列对实验现象的描述正确的是( )
| A. | 红磷在空气中燃烧,产生大量白烟 | |
| B. | 铁丝浸入稀盐酸,形成黄色溶液 | |
| C. | 持续加热碳酸氢铵,最终有固体残留 | |
| D. | 将浓硝酸滴入鸡蛋清,蛋清变黑 |
1.下列各组溶液,不用其他试剂就能鉴别的是( )
| A. | FeCl3 HCl NaOH KNO3 | B. | HCl K2CO3 CaCl2 BaCl2 | ||
| C. | MgSO4 BaCl2 CuSO4 Na2SO4 | D. | NH4Cl NaOH HCl Ca(OH)2 |
7.同学们整理实验室时,发现一瓶敞口放置且失去标签的白色粉末状药品,实验员老师告诉大家原瓶药品可能是碳酸钠,碳酸钙、氯化钠、氢氧化钠中的一种,同学们对此很好奇,于是他们对这瓶白色粉末的成分做了如下探究:
【实验Ⅰ】小明取一定量白色粉末于烧杯中,加水搅拌,充分溶解后,过滤,得到固体和无色溶液.
【实验Ⅱ】小明取实验Ⅰ得到的固体于试管中,滴加足量稀盐酸后,观察到有有气泡(现象)产生,于是小明马上就得出结论,该瓶中白色粉末一定是碳酸钙,但是小军却认为小明的结论不一定正确,固体还可能是碳酸钠,你认为小军的理由是碳酸钠的溶解度小,也会出现不溶性固体,请你写出上述有气体生成的反应的化学方程式Na2CO3+2HCl=2NaCl+H2O+CO2↑(任写一个).
【实验Ⅲ】小明和小军认为有必要再对实验Ⅰ中滤液的成分进行探究.过程如下:
【反思与交流】实验结束后,同学们通过讨论,一致认为原试剂瓶中的药品也可能不是碳酸钠,你认为他们的理由是氢氧化钠完全变质能生成碳酸钠.
【实际应用】某工厂化验室用15%的氢氧化钠溶液洗涤一定量石油产品中的残余硫酸,共消耗氢氧化钠溶液40g,洗涤后的溶液呈中性,这一定量石油产品中含H2SO4的质量是多少?
【实验Ⅰ】小明取一定量白色粉末于烧杯中,加水搅拌,充分溶解后,过滤,得到固体和无色溶液.
【实验Ⅱ】小明取实验Ⅰ得到的固体于试管中,滴加足量稀盐酸后,观察到有有气泡(现象)产生,于是小明马上就得出结论,该瓶中白色粉末一定是碳酸钙,但是小军却认为小明的结论不一定正确,固体还可能是碳酸钠,你认为小军的理由是碳酸钠的溶解度小,也会出现不溶性固体,请你写出上述有气体生成的反应的化学方程式Na2CO3+2HCl=2NaCl+H2O+CO2↑(任写一个).
【实验Ⅲ】小明和小军认为有必要再对实验Ⅰ中滤液的成分进行探究.过程如下:
| 实验步骤 | 实验现象 | 实验结论 |
| (1)取少量滤液于试管中,向其中滴加2-3滴无色酚酞试液,振荡 | 溶液由无色变为红色 | 该瓶中白色粉末一定不是碳酸钙和氯化钠 |
| (2)另取少量滤液于试管中,滴加过量氯化钙溶液,振荡,静置 | 产生白色沉淀 | 该瓶中白色粉末一定有碳酸钠,涉及的化学方程式为Na2CO3+CaCl2=2NaCl+CaCO3↓. |
【实际应用】某工厂化验室用15%的氢氧化钠溶液洗涤一定量石油产品中的残余硫酸,共消耗氢氧化钠溶液40g,洗涤后的溶液呈中性,这一定量石油产品中含H2SO4的质量是多少?