题目内容
【题目】如图为某同学所做的实验及现象。

(1)实验1中变浑浊的原因_____(文字叙述)。
(2)实验2生成Ca(HCO3)2,实验3发生反应的化学方程式为_____,该实验说明CaCO3比Ca(HCO3)2热稳定性_____(选填“强”或“弱”)。
(3)某地区硬水中溶有较多的可溶性Ca(HCO3)2、Mg(HCO3)2。
①生活中常用_____来区分硬水和软水。
②煮沸硬水可降低水的硬度,同时生成难溶性混合物固体A。
(猜想)固体A中除CaCO3外,还含有:
猜想1:只含MgCO3 猜想2:只含Mg (OH)2 猜想3:MgCO3和Mg (OH)2
(资料)MgCO3 +2HCl═MgCl2+H2O+CO2↑,Mg (OH)2 +2HCl═MgCl2+2H2O
(实验)取10.0g干燥的固体A,加入足量的稀盐酸充分反应,产生4.4gCO2气体。
(结论)①猜想1、2错误。其中判断猜想1错误的理由是_____。
【答案】二氧化碳与氢氧化钙反应生成碳酸钙白色沉淀和水 Ca(HCO3)2![]() CaCO3↓+CO2↑+H2O 强 肥皂水 若只含MgCO3,则生成的CO2大于4.4g
CaCO3↓+CO2↑+H2O 强 肥皂水 若只含MgCO3,则生成的CO2大于4.4g
【解析】
(1)二氧化碳与氢氧化钙反应生成碳酸钙白色沉淀和水,所以观察到澄清的石灰水变浑浊;故填:二氧化碳与氢氧化钙反应生成碳酸钙白色沉淀和水;
(2)在加热的条件下,碳酸氢钙分解为碳酸钙、水和二氧化碳,这说明CaCO3比Ca(HCO3)2热稳定性强;故填:Ca(HCO3)2![]() CaCO3↓+CO2↑+H2O;强;
CaCO3↓+CO2↑+H2O;强;
(3)
①区分硬水和软水的方法是:用肥皂水,加入肥皂水,泡沫多的是软水,泡沫少的是硬水;故填:肥皂水;
[资料]
①碳酸镁与盐酸反应生成氯化镁、二氧化碳和水;故填:MgCO3+2HCl=MgCl2+H2O+CO2↑;
[结论]
由化学方程式:
![]()
![]() 可知:
可知:
10.0g碳酸钙与足量的盐酸反应生成二氧化碳的质量为4.4g;10.0g碳酸镁与足量的稀盐酸反应生成二氧化碳的质量大于4.4g,氢氧化镁与盐酸反应不会生成二氧化碳;若只含MgCO3,则生成的CO2大于4.4g,所以猜想1错误;故填:若只含MgCO3,则生成的CO2大于4.4g。

【题目】掌握科学的研究方法,探索化学世界的奥秘。
(1)分类是学习化学的重要方法之一,生活中,常会接触到下列物质:
A 钢丝 B 甲烷 C 生石灰 D 碘酒
其中属于混合物的是_____(填字母,下同),属于氧化物的是_____。
(2)实验室中可用KClO3在MnO2催化下受热分解制取氧气,化学方程式为_____,将反应后的混合物进行分离。实验操作如图所示:
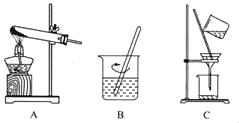
①图A中试管口略向下倾斜的原因是_____;
图B操作中玻璃棒的作用是_____;
图C操作中的一处明显错误是_____。
(3)质量守恒定律是帮助我们认识化学反应实质的重要理论。①下列表述正确的是_____。
A 蜡烛燃烧后质量减少,说明质量守恒定律不是普遍规律
B 每32gS和32gO2完全反应后,生成64gSO2
C 在化学反应aA+bB═cC+dD中一定有:a+b=c+d
②化合物R与足量氧气置于密闭容器中充分反应生成CO2和H2O,实验测得反应前后物质的质量如表:
R | O2 | CO2 | H2O | |
反应前质量/g | 46 | 128 | 0 | 0 |
反应后质量/g | 0 | 32 | x | 54 |
若参加反应的物质R与氧气的分子个数之比为1:3,则R的相对分子质量是_____。
【题目】碳酸氢钠是小苏打的主要成分,在生产和生活中有许多重要的用途。化学课上,同学们为了解碳酸氢钠的性质,将一定质量的碳酸氢钠和稀硫酸混合,充分反应后,有气体逸出,写出该反应的化学方程式_______,同学们对反应后溶液中溶质的成分进行了探究:认为除一定含有硫酸钠外可能还含有其他成分,因此进行了猜想并做了如下实验:
【实验用品】pH试纸、锌片、氧化铜粉末、稀硫酸、氢氧化钠溶液、氯化钡溶液。
【猜想与假设】反应后溶液中溶质的可能组成成分
猜想一:硫酸钠 猜想二:硫酸钠、碳酸氢钠 猜想三:硫酸钠、硫酸
【实验探究】同学们取反应后的溶液用不同方案进行如下实验,请根据结论完成下表实验现象中的①②③。
实验方案 | A | B | C | D | |
实验操作 |
|
|
|
| |
实验现象 | ① | 产生白色沉淀 | 试纸变色,对照标准比色卡,pH ②7 | ③ | |
实验结论 | 猜想二不正确 | 猜想三正确 | 猜想三正确 | 猜想三正确 | |
【得出结论】猜想三正确。
【评价反思】
(1)老师对同学们能用多种方案进行探究,并且得出正确的实验结论给予了肯定,同时指出探究中存在一处明显操作错误是:__________;
(2)有同学对实验方案B的结论提出了质疑,认为仅凭此现象不能得出猜想三正确,请说明理由________。
【总结提高】依据所给实验用品,设计不同的方案确认猜想三是正确的。请写出你的实验方案________。