题目内容
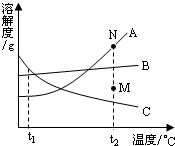
A、B、C三种物质的溶解度曲线如图所示,据图回答:①t1℃时,B物质的溶解度为 ;
②要将B物质从溶液中结晶出来,可采用的方法是 ;
③t1℃时,将12克C物质放入盛有40克水的烧杯中,所得的溶液质量是 克;
④若将等质量A、B、C三种物质的饱和溶液从t1℃升至t2时,所得溶液的溶质质量分数由大到少的顺序为: .

【答案】分析:①根据固体物质的溶解度曲线可知某温度下物质的溶解度;
②固体物质从溶液中结晶析出的方法有蒸发溶剂和降温结晶两种方法,溶解度受温度变化较小的物质可采用蒸发溶剂的方法,溶解度受温度变化较大的物质可采用降温结晶的方法;
③根据t1℃时C物质的溶解度分析解答;
④根据固体物质的溶解度曲线可以比较不同物质在同一温度下的溶解度大小;升高温度,AB变为不饱和溶液,C变为饱和溶液,进而比较溶质的质量分数大小.
解答:解:①观察溶解度曲线可知:t1℃时,B物质的溶解度为40g或40g/100g水;
故答案为:40g或40g/100g水;
②从图中可以看出,B物质的溶解度受温度变化较小,可采用蒸发溶剂的方法;
故答案为:蒸发溶剂;
③t1℃时C物质的溶解度是25g,所以40g水最多溶解10gC物质,所得溶液的质量是50g;
故答案为:50;
④将等质量A、B、C三种物质的饱和溶液,从t1℃升至t2时,AB变为不饱和溶液,所以其溶解的物质和t1℃时相同,即溶质的质量分数和t1℃时相同,C的溶解度变小,变为饱和溶液,根据饱和时溶质的质量分数的计算式: ×100%,即溶解度越大溶质的质量分数也就越大,所以此时溶液的质量分数关系是B>A>C;
×100%,即溶解度越大溶质的质量分数也就越大,所以此时溶液的质量分数关系是B>A>C;
故答案为:B>A>C.
点评:从溶解度曲线可以看出:同一溶质在不同温度下的溶解度;同一温度下,不同溶质的溶解度;温度对不同物质的溶解度影响不同.
②固体物质从溶液中结晶析出的方法有蒸发溶剂和降温结晶两种方法,溶解度受温度变化较小的物质可采用蒸发溶剂的方法,溶解度受温度变化较大的物质可采用降温结晶的方法;
③根据t1℃时C物质的溶解度分析解答;
④根据固体物质的溶解度曲线可以比较不同物质在同一温度下的溶解度大小;升高温度,AB变为不饱和溶液,C变为饱和溶液,进而比较溶质的质量分数大小.
解答:解:①观察溶解度曲线可知:t1℃时,B物质的溶解度为40g或40g/100g水;
故答案为:40g或40g/100g水;
②从图中可以看出,B物质的溶解度受温度变化较小,可采用蒸发溶剂的方法;
故答案为:蒸发溶剂;
③t1℃时C物质的溶解度是25g,所以40g水最多溶解10gC物质,所得溶液的质量是50g;
故答案为:50;
④将等质量A、B、C三种物质的饱和溶液,从t1℃升至t2时,AB变为不饱和溶液,所以其溶解的物质和t1℃时相同,即溶质的质量分数和t1℃时相同,C的溶解度变小,变为饱和溶液,根据饱和时溶质的质量分数的计算式:
 ×100%,即溶解度越大溶质的质量分数也就越大,所以此时溶液的质量分数关系是B>A>C;
×100%,即溶解度越大溶质的质量分数也就越大,所以此时溶液的质量分数关系是B>A>C;故答案为:B>A>C.
点评:从溶解度曲线可以看出:同一溶质在不同温度下的溶解度;同一温度下,不同溶质的溶解度;温度对不同物质的溶解度影响不同.

练习册系列答案
 暑假作业海燕出版社系列答案
暑假作业海燕出版社系列答案 本土教辅赢在暑假高效假期总复习云南科技出版社系列答案
本土教辅赢在暑假高效假期总复习云南科技出版社系列答案 暑假作业北京艺术与科学电子出版社系列答案
暑假作业北京艺术与科学电子出版社系列答案
相关题目
 6、下图为A、B、C三种物质的溶解度曲线,试回答下列问题:
6、下图为A、B、C三种物质的溶解度曲线,试回答下列问题: (2013?广东模拟)“
(2013?广东模拟)“ ”、“
”、“ ”、“
”、“ ”分别表示A、B、C三种物质的原子,下列关于如图说法正确的是( )
”分别表示A、B、C三种物质的原子,下列关于如图说法正确的是( )
 (2012?吴中区三模)如图是a、b、c三种物质的溶解度曲线,回答下列问题:
(2012?吴中区三模)如图是a、b、c三种物质的溶解度曲线,回答下列问题: