题目内容
11.实验室用200g稀硫酸和30g粗锌(杂质不与酸反应,也不溶于水)恰好完全反应,制得0.8g氢气,求:(1)粗锌的纯度是多少;
(2)稀硫酸的溶质质量分数是多少;
(3)反应后所得溶液中的溶质质量分数是多少?
分析 锌和稀硫酸反应生成硫酸锌和氢气,根据氢气质量可以计算锌、硫酸和硫酸锌的质量,进一步可以计算粗锌的纯度、稀硫酸的溶质质量分数、反应后所得溶液中的溶质质量分数.
解答 解:(1)设锌的质量为x,硫酸质量为y,生成硫酸锌质量为z,
Zn+H2SO4═ZnSO4+H2↑,
65 98 161 2
x y z 0.8g
$\frac{65}{x}$=$\frac{98}{y}$=$\frac{161}{z}$=$\frac{2}{0.8g}$,
x=26g,y=39.2g,z=64.4g,
粗锌的纯度是:$\frac{26g}{30g}$×100%=86.7%,
答:粗锌的纯度是86.7%.
(2)稀硫酸的溶质质量分数是:$\frac{39.2g}{200g}$×100%=19.6%,
答:稀硫酸的溶质质量分数是19.6%.
(3)反应后所得溶液中的溶质质量分数是:$\frac{64.4g}{26g+200g-0.8g}$×100%=28.6%,
答:反应后所得溶液中的溶质质量分数是28.6%.
点评 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
 英才点津系列答案
英才点津系列答案 红果子三级测试卷系列答案
红果子三级测试卷系列答案 课堂练加测系列答案
课堂练加测系列答案
相关题目
2.5月31日是“世界无烟日”.吸烟对人体有害,吸烟产生的气体中含有一种能与血液中血红蛋白结合的有毒气体,它是( )
| A. | CO2 | B. | SO2 | C. | CO | D. | H2O |
1.某加碘精制盐标签如图所示,下列关于该加碘精制盐说法中错误的是( )

| A. | 该加碘精制盐为混合物 | |
| B. | 该加碘精制盐中含有碘单质 | |
| C. | 该加碘精制盐中含有两种化合物 | |
| D. | 一包该加碘精制盐中含有碘的质量为10-25mg |
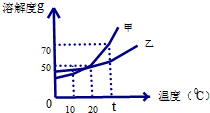 观察图甲、乙两种物质的溶解度曲线回答问题
观察图甲、乙两种物质的溶解度曲线回答问题