题目内容
在浓硫酸的催化作用下,固体草酸(H2C2O4)受热分解生成碳的氧化物和水。某化学课外兴趣小组对碳的氧化物的成分进行了实验探究。
【提出问题】如何通过实验确定碳的氧化物的成分。
【收集资料】a.浓硫酸有吸水性,可用于干燥某些气体;
b.氢氧化钠溶液可与CO2反应,可除去CO2气体。
【猜 想】
| 猜 | 猜想2 | 猜想3 |
| 只有CO | 只有 | CO和CO2都有 |
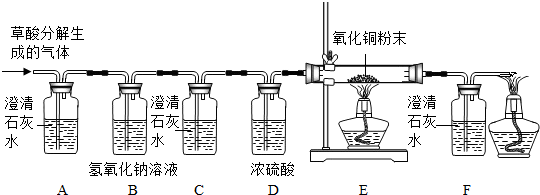
【设计实验】基于猜想3 ,兴趣小组同学设计了如下实验装置:
,兴趣小组同学设计了如下实验装置:
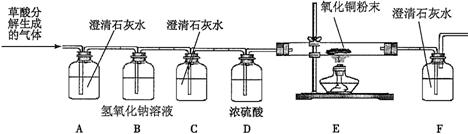
【实验探究】
① 实验过 程中观察到 (14) 装置(填字母)中的澄清石灰水变浑浊,证明有CO2气体。
程中观察到 (14) 装置(填字母)中的澄清石灰水变浑浊,证明有CO2气体。
② 实验过程中还观察到以下实验现象:I.C装置中澄清石灰水不变浑浊;II.E装置中
黑色粉末变成红色;III. (15) ,证明有CO气体。
【实验结论】通过实验探究证明:猜想3成立。
草酸分解的化学方程式是 (16) 。
【问题讨论】
① C装置的作用是 (17) ;
② 该实验装置还需完善之处是 (18) 。
【计算】若有4.4g的二氧化碳通入到足量的澄清石灰水中,则理论上可以产生多少摩尔沉淀?(根据化学方程式列式计算 (19)
(13)CO2 (14)A (15) F中澄清的石灰水变浑浊
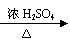 (16)H2C2O4
(16)H2C2O4 CO↑+CO2↑+H2O
CO↑+CO2↑+H2O
(17)检验CO2是否除尽 (18)酒精灯点燃F装置中的尾气
(19)n(CO2)=4.4/44=0.1mol
设可以产生xmol沉淀
CO2+Ca(OH)2→ CaCO3↓+H2O
1 1
0.1 x
1/0.1=1/x
x=0.1mol
答:理论上可以产生0.1摩尔沉淀。

 百年学典课时学练测系列答案
百年学典课时学练测系列答案 仁爱英语同步练习册系列答案
仁爱英语同步练习册系列答案