题目内容
16.在20℃时,将Ca(NO3)2和KNO3的混合物26.2克,放入56.2亚克水中使其完全溶解,然后加入27.6克溶质质量分数为50%的K2CO3溶液,恰好完全反应(已知20℃时KNO3的溶解度为31.6克,K2CO3的溶解度为110.5克).试求:(1)生成碳酸钙的质量;
(2)反应后所得溶液中溶质的质量分数(最后结果保留二位小数).
分析 根据硝酸钙和碳酸钾反应会生成碳酸钙沉淀和硝酸钾,结合题中的数据进行分析解答.
解答 解:设生成碳酸钙质量为x,参加反应的硝酸钙质量为y,反应中生成的硝酸钾质量为z,
Ca(NO3)2+K2CO3=CaCO3↓+2KNO3
164 138 100 202
y 27.6g×50% x z
$\frac{164}{y}$=$\frac{138}{27.6g×50%}$=$\frac{100}{x}$=$\frac{202}{z}$
x=10g
y=16.4g
z=20.2g
(1)生成碳酸钙质量为10g;
(2)反应后所得溶液中硝酸钾的质量为:20.2g+(26.2-16.4)g=30g
反应后所得溶液中水的质量为:56.2g+27.6g×50%=70g
设20℃70g水最多溶解硝酸钾质量为m
$\frac{100g}{31.6g}$=$\frac{70g}{m}$
m=22.12g<30g
所以硝酸钾没有完全溶解
所以所得硝酸钾的溶质质量分数为:$\frac{22.12g}{70g+22.12g}$×100%=24%.
故答案为:(1)10g;
(2)24%.
点评 本题主要考查了化学方程式的有关运算,难度不大,注意计算溶液质量分数时,需要考虑固体是否全部溶解.

练习册系列答案
相关题目
6.下列图示中正确的是( )
| A. |  滴加溶液 | B. | 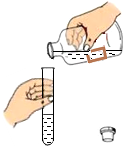 倾倒液体 | ||
| C. | 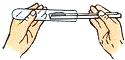 用纸槽往试管里送入固体粉末 | D. | 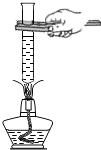 给试管里的液体加热 |
7.以下的反应,既不是化合反应,又不是分解反应的是( )
| A. | 水+二氧化碳→碳酸 | B. | 铜+水+二氧化碳+氧气→碱式碳酸铜 | ||
| C. | 锌+硫酸→硫酸锌+氢气 | D. | 碳酸氢铵→二氧化碳+氨气 |
4.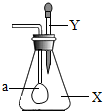 如图所示,锥形瓶内盛有气体X,滴管内盛有液体Y,若挤压胶头滴管使液体滴入瓶中,振荡,一会儿可见小气球a鼓起.X、Y可能是哪些物质?请将相应物质的化学式填入下表中:
如图所示,锥形瓶内盛有气体X,滴管内盛有液体Y,若挤压胶头滴管使液体滴入瓶中,振荡,一会儿可见小气球a鼓起.X、Y可能是哪些物质?请将相应物质的化学式填入下表中:
 如图所示,锥形瓶内盛有气体X,滴管内盛有液体Y,若挤压胶头滴管使液体滴入瓶中,振荡,一会儿可见小气球a鼓起.X、Y可能是哪些物质?请将相应物质的化学式填入下表中:
如图所示,锥形瓶内盛有气体X,滴管内盛有液体Y,若挤压胶头滴管使液体滴入瓶中,振荡,一会儿可见小气球a鼓起.X、Y可能是哪些物质?请将相应物质的化学式填入下表中:| X | Y |
| CO2 | NaOH |
| NH3 | H2SO4 |
5.实验室利用下列反应原理制取有关气体,不合理的是( )
| A. | 制取02:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$ K2MnO4+MnO2+O2↑ | |
| B. | 制取H2:Zn+2HCl═ZnCl2+H2↑ | |
| C. | 制取C02:CaCO3+H2SO4═CaSO4+CO2↑+H2O | |
| D. | 制取02:2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑ |