题目内容
水和以水为溶剂制成的溶液,与人们的生活有着密切的关系.

(1)近几年我国不少水域多次发生严重的“赤潮”、“水华”现象.“赤潮”、“水华”主要是水面上的藻类疯狂生长、繁殖,水质恶化.已知某种藻类的化学式为C106H263O110N16P,该物质分子中碳、氮原子个数比________.
(2)配制500g生理食盐水(溶质的质量分数是0.9%)需要水的质量是________.
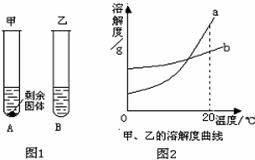
(3)20℃时,分别向盛有10g水的两支试管中,加入质量的甲、乙两种固体物质,使其充分溶解,可观察到如图所示的现象.
①20℃时,________(填“A”或“B”)试管中的溶液一定是饱和溶液;
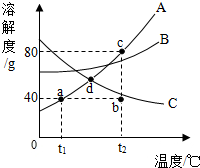
②如图2中表示甲物质的溶解度曲线的是________(填“a”或“b”),要使A试管中剩余的固体继
续溶解可采用的方法是________.
(4)A、B、C是初中常见的物质,其中B为水,写出A→B属于复分解反应 的化学方程式:________.

解:(1)由题目中所给物质的化学式,可以看出每个分子中碳原子的个数为106,氮原子的个数为16,然后得出碳、氮原子个数比,故答案为:53:8;
(2)由溶质质量分数的计算公式可得:氯化钠的质量为:500g×0.9%=4.5g,由溶液质量=溶质质量+溶剂质量得,水的质量为:500g-4.5g=495.5g,故答案为:495.5g;
(3)①A试管中的甲有固体剩余,所以一定为饱和溶液,乙试管中无固体剩余,可能是不饱和溶液,也可能是恰好饱和,故答案为:A;
②根据图一中现象,可以得出20℃时甲的溶解度小于乙的溶解度,由图2进行查阅可得,20℃时b的溶解度小于a的溶解度,即可确定b表示甲物质的溶解度曲线.要使A试管中剩余的固体继续溶解,因b溶解度随温度升高而增大,所以可用降低温度法,另外还可加水.故答案为:b; 加水或升温.
(4)复分解反应生成水的物质有:酸碱反应、酸与碳酸盐反应、酸与金属氧化物反应碱与铵盐反应,可选取其一进行书写,故答案为:NaOH+HCl═NaOH+H2O或Na2CO3+2HCl=2NaCl+H2O+CO2↑(合理即可)
分析:(1)题目中所给物质的化学式,由下标确定每个分子中每种原子的个数,然后得出碳、氮原子个数比;
(2)依据溶质质量分数的计算公式、溶液质量=溶质质量+溶剂质量进行计算,得出答案;
(3)①依据试管中的现象判断溶液是否一定是饱和溶液,若无固体剩余,可能是不饱和溶液,也可能是恰好饱和,若有固体剩余,则一定为饱和溶液;
②依据图一中现象,比较出20℃时甲乙两种物质的溶解度特点,再根据图2比较出20℃时ab的溶解度特点,即可确定出表示甲物质的溶解度曲线.要使A试管中剩余的固体继续溶解,根据其溶解度变化确定升温还是降温,另外还可加水;
(4)依据B为水及反应类型为复分解反应确定反应的化学方程式,可以从哪些物质间的反应是复分解反应入手进行判断.
点评:该题以信息形式考查了化学式的计算、溶解度曲线的利用、溶质质量分数的计算、化学方程式的书写,涉及的知识点多,有一定思维容量,解答时应看清每小题考查的不同知识点,利用所学对应知识进行分析判断.
(2)由溶质质量分数的计算公式可得:氯化钠的质量为:500g×0.9%=4.5g,由溶液质量=溶质质量+溶剂质量得,水的质量为:500g-4.5g=495.5g,故答案为:495.5g;
(3)①A试管中的甲有固体剩余,所以一定为饱和溶液,乙试管中无固体剩余,可能是不饱和溶液,也可能是恰好饱和,故答案为:A;
②根据图一中现象,可以得出20℃时甲的溶解度小于乙的溶解度,由图2进行查阅可得,20℃时b的溶解度小于a的溶解度,即可确定b表示甲物质的溶解度曲线.要使A试管中剩余的固体继续溶解,因b溶解度随温度升高而增大,所以可用降低温度法,另外还可加水.故答案为:b; 加水或升温.
(4)复分解反应生成水的物质有:酸碱反应、酸与碳酸盐反应、酸与金属氧化物反应碱与铵盐反应,可选取其一进行书写,故答案为:NaOH+HCl═NaOH+H2O或Na2CO3+2HCl=2NaCl+H2O+CO2↑(合理即可)
分析:(1)题目中所给物质的化学式,由下标确定每个分子中每种原子的个数,然后得出碳、氮原子个数比;
(2)依据溶质质量分数的计算公式、溶液质量=溶质质量+溶剂质量进行计算,得出答案;
(3)①依据试管中的现象判断溶液是否一定是饱和溶液,若无固体剩余,可能是不饱和溶液,也可能是恰好饱和,若有固体剩余,则一定为饱和溶液;
②依据图一中现象,比较出20℃时甲乙两种物质的溶解度特点,再根据图2比较出20℃时ab的溶解度特点,即可确定出表示甲物质的溶解度曲线.要使A试管中剩余的固体继续溶解,根据其溶解度变化确定升温还是降温,另外还可加水;
(4)依据B为水及反应类型为复分解反应确定反应的化学方程式,可以从哪些物质间的反应是复分解反应入手进行判断.
点评:该题以信息形式考查了化学式的计算、溶解度曲线的利用、溶质质量分数的计算、化学方程式的书写,涉及的知识点多,有一定思维容量,解答时应看清每小题考查的不同知识点,利用所学对应知识进行分析判断.

练习册系列答案
相关题目
水和以水为溶剂制成的溶液,与人们的生活有着密切的关系。
(1)生理盐水中的溶剂是 。
(2)市售的一种罐装饮料,在饮料罐的夹层中分别装入一种固体物质和水,饮用前摇动饮料罐使它们混合,饮料温度就会降低,这种固体物质可能是 (填字母)。
A.烧碱 B.食盐 C.硝酸铵 D.生石灰
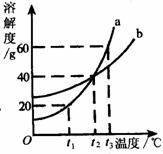
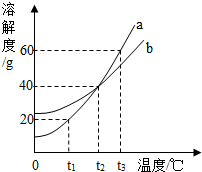
(3)右图为a、b两种固体物质的溶解度曲线,请依据曲线图回答问题:
①在t3℃时,50g水中最多能够溶解a物质的质量是 ;
②在 ℃时,a物质的饱和溶液和b物质的饱和溶液中,溶质的质量分数相等。
③把100g质量分数为20%的a溶液从t3℃降温到t2℃,此时a溶液的质量分数是 。
(4)现有一瓶浓硫酸,标签如图所示。欲将该瓶浓硫酸完全稀释成20%的稀硫酸,需要水的质量是 g。
|

 (2013?塘沽区一模)水和以水为溶剂制成的溶液,与人们的生活有着密切的关系.
(2013?塘沽区一模)水和以水为溶剂制成的溶液,与人们的生活有着密切的关系.
