题目内容
银白色的镁条表面常有一层灰黑色的“外衣”,某小组同学进行了如下探究:
I.甲同学认为该外衣是MgO,遭到否定,否定的理由是____________.
Ⅱ.查阅资料:镁条变黑是因为生成了碱式碳酸镁[Mgx(OH)yCO3]。
探究1:影响镁条变黑的因素
(1)根据碱式碳酸镁含有H元素,推测镁条变黑与空气中的_______有关;
(2)根据碱式碳酸镁含有C元素,推测镁条变黑与空气中的_______有关;
(3)为确认镁条变黑是否与O2有关,乙同学设计了如下实验:
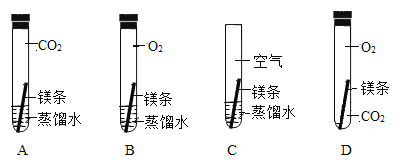
同学们讨论得出:只要完成实验_______和_______(选填序)就可达到探究目的。
探究2:碱式碳酸镁[Mgx(OH)yCO3]的化学式
(资料)①碱式碳酸镁受热分解生成三种氧化物;
②NaOH溶液吸收CO2,浓H2SO4只吸收水。
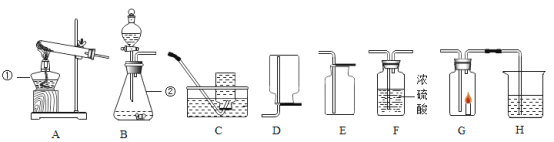
(实验)将1.42g碱式碳酸镁加热至完全分解,使产生的气体全部缓缓通过下图装置,测定生成气体的质量(假设每步吸收均完全)。

(数据)①浓硫酸增重0.18g;②NaOH 溶液增重0.44g。
(结论)x:y=____:______,碱式碳酸镁受热分解的化学方程式为_________。
(延伸)工业上碱式碳酸镁可作阻燃剂,其可能的原因是_________(选填序号)。
a分解时吸热,降低可燃物的着火点
b生成的固体覆盖燃烧物,隔绝氧气
c生成的气体稀释了可燃物周围的氧气浓度
 课堂练加测系列答案
课堂练加测系列答案 轻松课堂单元测试AB卷系列答案
轻松课堂单元测试AB卷系列答案碱式碳酸锌的组成测定。为确定碱式碳酸锌[aZnCO3·bZn(OH)2·cH2O]的组成,现称取35.9g样品进行如下实验。

(资料)①Zn(OH)2加热至125℃、ZnCO3加热至350℃分别分解生成两种氧化物。该碱式碳酸锌失去结晶水的温度与Zn(OH)2的分解温度接近。
②浓硫酸具有吸水性,NaOH溶液能充分吸收CO2,碱石灰能充分吸收CO2和H2O。
(1)装配好实验装置后,先要______________。
(2)加热前后及过程中均通入氮气,停止加热后继续通氮气的目的是___________。
(3)控制温度在不同的范围对A中样品加热。测得装置B、C的质量在实验前后的变化情况如下表所示,测得A中剩余固体质量随温度的变化如下图所示。
装置 | 实验前/g | 实验后/g |
B | 198.0 | 205.2 |
C | 221.0 | 225.4 |

①m=________g。
②a:b:=_________。
③如缺少装置D,会导致________(选填“a”、“b”或“c”)测定结果偏大。


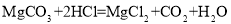 。将MgCO3和CaCO3的混合物ag加入足量的100.0g稀盐酸中,固体完全溶解。将产生的CO2通入足量澄清石灰水,充分反应后产生沉淀10.0g。下列说法错误的是
。将MgCO3和CaCO3的混合物ag加入足量的100.0g稀盐酸中,固体完全溶解。将产生的CO2通入足量澄清石灰水,充分反应后产生沉淀10.0g。下列说法错误的是