��Ŀ����
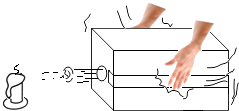
����Ŀ��ij��ȤС��Ϊ�ⶨʵ������һƿ���õĹ���������Һ�����ʵ�����������ʵ���������������ͼ��ʾ�� 
��1��ʣ��Ļ�����ж������̵�����Ϊg����Ӧ��������������Ϊg��
��2������ù���������Һ����������������
��3��ʵ���������ͭ��Һ�ڸ÷�Ӧ��Ҳ���������̵����ã�����5.6g��ˮ����ͭ����������̽��б�ʵ�飬����ʣ�����Һ�����ʵ����������� ������ͭȫ������ˮ������ʱ������0.1%��
���𰸡�
��1��1.0��1.6
��2���⣺��68.0g����������Һ�к��й������������Ϊx��
2H2O2 | O2�� |
68 | 32 |
x | 1.6g |
![]() =
= ![]() x=3.4g
x=3.4g
����������Һ�����ʵ���������= ![]() ��100%=5.0%
��100%=5.0%
��3���⣺����ͭ��Һ��������������= ![]() ��100%��7.8%
��100%��7.8%
���������⣺��1�� ��Ӧ�д������������ڷ�Ӧǰ���������䣬��Ϊ1.0g�����������غ㶨�ɣ���Ӧ��������������=68.0g+1.0g��67.4g=1.6g��
���Դ��ǣ�1.0��1.6���𣺣�2������ù���������Һ��������������5.0%����3��ʣ�����Һ�����ʵ���������ԼΪ7.8%��
�����㾫����������Ҫ�����������غ㶨�ɼ���Ӧ�ú��ݻ�ѧ��Ӧ����ʽ�ļ�������֪ʶ�㣬��Ҫ���բ������غ㶨��ֻ�����ڻ�ѧ�仯���������������仯���ڲ��μӷ�Ӧ����������������������������������ܼ��롰�ܺ͡��У���Ҫ���ǿ����е������Ƿ�μӷ�Ӧ�����ʣ������壩������©�������ʼ�������=ϵ������Է�������֮�Ȳ�����ȷ�����⣮