题目内容
 (2013?潮阳区模拟)如图是某品牌补铁剂的标签.请回答:
(2013?潮阳区模拟)如图是某品牌补铁剂的标签.请回答:(1)富马酸亚铁颗粒中的铁属于
微量
微量
元素(填“常量”或“微量”);(2)富马酸亚铁中C、H元素的质量比为
24:1
24:1
;富马酸亚铁的相对分子质量为170
170
;(3)富马酸亚铁(C4H2FeO4)中铁元素的质量分数为
33%
33%
,若每次服用1包该补铁剂,摄入铁元素的质量为(取整数)66
66
mg.分析:(1)根据人体内常量元素与微量元素的种类进行分析判断.
(2)根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比、相对分子质量为构成分子的各原子的相对原子质量之和,进行分析解答.
(3)根据化合物中元素的质量分数=
×100%、化合物中某元素的质量=该化合物的质量×该元素的质量分数,进行分析解答.
(2)根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比、相对分子质量为构成分子的各原子的相对原子质量之和,进行分析解答.
(3)根据化合物中元素的质量分数=
| 相对原子质量×原子个数 |
| 相对分子质量 |
解答:解:(1)人体中的常量元素主要有:氧、碳、氢、氮、钙、磷、钾、硫、钠、氯、镁;微量元素主要有:铁、钴、铜、锌、铬、锰、钼、氟、碘、硒,铁元素属于微量元素.
(2)富马酸亚铁中碳、氢两种元素的质量比为(12×4):(1×2)=24:1;富马酸亚铁的相对分子质量为12×4+1×2+56+16×4=170.
(3)富马酸亚铁(C4H2FeO4)中铁元素的质量分数为
×100%≈33%;由题意,每包含富马酸亚铁0.2g,若每次服用1包该补铁剂,摄入铁元素的质量为(取整数)0.2g×33%=0.066g
=66mg.
故答案为:(1)微量;(2)24:1;170;(3)33%;66.
(2)富马酸亚铁中碳、氢两种元素的质量比为(12×4):(1×2)=24:1;富马酸亚铁的相对分子质量为12×4+1×2+56+16×4=170.
(3)富马酸亚铁(C4H2FeO4)中铁元素的质量分数为
| 56 |
| 170 |
=66mg.
故答案为:(1)微量;(2)24:1;170;(3)33%;66.
点评:本题难度不大,考查同学们结合标签新信息、灵活运用化学式的有关计算进行分析问题、解决问题的能力.

练习册系列答案
 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案
相关题目

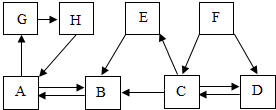 (2013?潮阳区模拟)如图所示是初中化学中几种常见物质之间的相互转化关系(部分反应物和生成物及反应条件已略去).化合物A、G、H含有相同的金属元素,在常温下,B、C为气体,B是植物光合作用的重要原料;D、F是由两种相同元素组成的无色液体,分子中的原子个数比为2:1和1:1;E为黑色固体,与稀硫酸反应得到蓝色溶液.回答下列问题:
(2013?潮阳区模拟)如图所示是初中化学中几种常见物质之间的相互转化关系(部分反应物和生成物及反应条件已略去).化合物A、G、H含有相同的金属元素,在常温下,B、C为气体,B是植物光合作用的重要原料;D、F是由两种相同元素组成的无色液体,分子中的原子个数比为2:1和1:1;E为黑色固体,与稀硫酸反应得到蓝色溶液.回答下列问题:
