题目内容
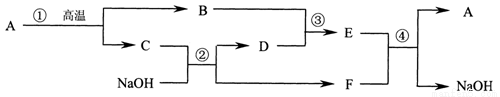
(7分)已知NaOH容易与空气中的CO2作用而变质。小军同学在实验室发现一瓶敞口放置的NaOH固体后,设计方案,对这瓶NaOH固体变质情况进行了如下实验探究:

回答下列问题:
(1)上述实验操作④的名称是: 。
(2)根据上述实验,可以确定该固体 变质。
(3)步骤③中加过量氯化钙溶液的目的是 。
(4)若测得E的PH=7,则A的成分 (写化学式),若测得E的PH>7,则A的成分 (写化学式)。
(5)实验室有一瓶久罝的氢氧化钠,因吸收空气中二氧化碳而变质,经测定该固体中碳元素的质量分数为6%。则已变质的氢氧化钠占变质前纯氢氧化钠的质量分数为 (保留整数).
(1)过滤;(2)已 (3)除尽碳酸钠;(4)NaOH NaOH和Na2CO3 (5)46%
【解析】
试题分析:实验操作④能得到沉淀说明是过滤;加入氯化钙产生沉淀说明物质含有碳酸根,因此说明已经变质;步骤③中加过量氯化钙溶液的目的是除尽碳酸钠并且检验是否变质;测得E的PH=7,则A的成分是NaOH;若测得E的PH>7,则A的成分是NaOH和Na2CO3。设固体的质量为100克,则含有的碳元素的质量为6克,则变质后的碳酸钠的质量=6÷(12/106×100%)=53克,设生成53克碳酸钠需要氢氧化钠的质量为X,根据配平的方程式得到这样的关系:2 NaOH~Na2CO3
80 106
X 53克
列比例式得:80:X=106:53 X=40克
总的氢氧化钠的质量=40克+(100克-53克)=87克
已变质的氢氧化钠占变质前纯氢氧化钠的质量分为=40/87×100%≈46%。
考点:氢氧化钠的性质和变化 物质的质量分数的计算 根据化学方程式的计算

为除去下列物质中混有的少量的杂质,所用试剂正确的是
物质 | 杂质 | 所用试剂、方法 | |
A. | N2 | O2 | 通过灼热CuO |
B. | CaO | CaCO3 | 高温煅烧 |
C. | CO2 | H2O | 通过NaOH固体 |
D. | FeCl2 溶液 | CuCl2 | 加入过量铁粉、过滤 |