题目内容
奥运火炬燃烧时主要是将化学能转变成________能和光能;火炬铝柄表面有一层致密的氧化铝保护膜,它是常温下铝与氧气反应生成的,该反应的化学方程式为:________.
热 4Al+3O2=2 Al2O3
分析:此题较简单,在燃烧火炬时是将化学能转变为热能和光能.铝在发生变化时是常温,所以不用加热符号.
解答:奥运火炬燃烧时主要是将化学能转变成热能和光能
发生反应的化学方程式为4Al+3O2=2 Al2O3
点评:铝的表面形成致密的保护膜时的方程式在书写时注意配平,这是这一题出错较高的地方.
分析:此题较简单,在燃烧火炬时是将化学能转变为热能和光能.铝在发生变化时是常温,所以不用加热符号.
解答:奥运火炬燃烧时主要是将化学能转变成热能和光能
发生反应的化学方程式为4Al+3O2=2 Al2O3
点评:铝的表面形成致密的保护膜时的方程式在书写时注意配平,这是这一题出错较高的地方.

练习册系列答案
 华东师大版一课一练系列答案
华东师大版一课一练系列答案
相关题目
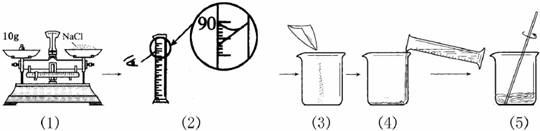
某化学兴趣小组对“氢氧化钠与稀盐酸反应中溶液温度升高的现象”进行了实验探究.在一定体积10%的氢氧化钠溶液中滴加10%的盐酸,并对反应中溶液的温度与加入盐酸的体积变化记录如下:
| 加入盐酸体积V(mL) | 0 | 2 | 6 | 10 | 16 | 20 |
| 测得溶液温度t℃ | 14.0 | 15.2 | 22.0 | 28.2 | 24.7 | 22.9 |

请回答下列问题:
(1)写出氢氧化钠与稀盐酸反应的化学方程式________.
(2)在如图中,绘出溶液的温度与加入盐酸的体积之间的变化关系曲线.
(3)根据实验可得出结论是________.
(4)根据曲线讨论溶液温度变化的原因.加入盐酸的量在2-10mL之间时:________;加入盐酸的量在lO-20mL之间时:________.
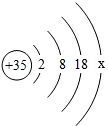 ,溴原子核外共有________个电子,最外层上的x数值为________.
,溴原子核外共有________个电子,最外层上的x数值为________.