题目内容
“南海一号”上发现的铜钱已经生锈,有少量铜绿[Cu2(OH)2CO3]附着,铜绿在加热时能生成三种氧化物.则该反应的化学方程式为______ 2CuO+2H2O+CO2↑
【答案】分析:根据质量守恒定律和题目信息推测铜绿加热的化学方程式,判断反应类型;根据常见的还原剂填写.
解答:解:根据质量守恒定律和三种氧化物可知,三种氧化物应该是氧化铜、水、二氧化碳,在书写化学方程式时注意反应的条件和配平以及气体符号:Cu2(OH)2CO3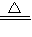 2CuO+H2O+CO2↑;,该反应由一种物质生成三种物质,属于分解反应;生成物中黑色氧化铜生成红色的铜,需加入还原剂,常见的还原剂有氢气、一氧化碳和碳.
2CuO+H2O+CO2↑;,该反应由一种物质生成三种物质,属于分解反应;生成物中黑色氧化铜生成红色的铜,需加入还原剂,常见的还原剂有氢气、一氧化碳和碳.
故答案为:Cu2(OH)2CO3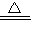 2CuO+2H2O+CO2↑,分解反应. H2、CO、C.
2CuO+2H2O+CO2↑,分解反应. H2、CO、C.
点评:解答本题要充分理解铜绿受热分解的实质等方面的知识,只有这样才能正确书写化学方程式.
解答:解:根据质量守恒定律和三种氧化物可知,三种氧化物应该是氧化铜、水、二氧化碳,在书写化学方程式时注意反应的条件和配平以及气体符号:Cu2(OH)2CO3
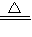 2CuO+H2O+CO2↑;,该反应由一种物质生成三种物质,属于分解反应;生成物中黑色氧化铜生成红色的铜,需加入还原剂,常见的还原剂有氢气、一氧化碳和碳.
2CuO+H2O+CO2↑;,该反应由一种物质生成三种物质,属于分解反应;生成物中黑色氧化铜生成红色的铜,需加入还原剂,常见的还原剂有氢气、一氧化碳和碳.故答案为:Cu2(OH)2CO3
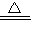 2CuO+2H2O+CO2↑,分解反应. H2、CO、C.
2CuO+2H2O+CO2↑,分解反应. H2、CO、C.点评:解答本题要充分理解铜绿受热分解的实质等方面的知识,只有这样才能正确书写化学方程式.

练习册系列答案
 优学名师名题系列答案
优学名师名题系列答案
相关题目