题目内容
19.中和反应是酸与碱生成盐和水的反应,请你回答以下问题:(1)下列事实不能表明盐酸与氢氧化钠一定发生了化学反应的是A;
A.向氢氧化钠固体中加入盐酸后,混合溶液的温度升高
B.向氢氧化钠溶液中加入一定量盐酸后,混合溶液中的溶质变成氢氧化钠和氯化钠
C.向滴有酚酞的盐酸中加入氢氧化钠溶液后,酚酞没有变色
D.向氢氧化钠溶液中加入一定量的盐酸后,混合溶液的pH<7
(2)化学兴趣小组在进行酸碱中和反应的课外研究时做了如下实验:向装有50g稀硫酸的小烧杯中,慢慢滴加Ba(OH)2饱和溶液至过量,并测定了其溶液的温度、电导率变化曲线,请回答以下问题:

①请写出稀硫酸与氢氧化钡溶液反应的化学方程式H2SO4+Ba(OH)2=BaSO4↓+2H2O;
②稀硫酸溶液能导电,是因为其溶液中有自由移动的H+、SO42-(填微粒符号),从图中可以看出当加入质量为m2g的Ba(OH)2溶液时,溶液导电性几乎为0;
③经过实验探究他们对中和反应的现象进行了归类并提出猜想:
Ⅰ.酸碱溶液混合时有的无明显现象,如氢氧化钠溶液与稀盐酸混合;
Ⅱ.酸碱溶液混合时有的会产生白色沉淀,如氢氧化钡溶液与稀硫酸混合;
Ⅲ.请你模仿Ⅰ和Ⅱ,再举一种酸碱中和有明显现象的实例(用化学方程式表示)H2SO4+Cu(OH)2=CuSO4+2H2O.
分析 (1)物质发生化学反应时经常伴随发生一些现象,如发光,放热,变色,生成气体、沉淀等.根据这些现象可帮助我们判断物质是否发生了化学反应.
(2)①根据硫酸和氢氧化钡溶液反应生成硫酸钡沉淀和水进行解答;
②根据硫酸电离时会生成氢离子与硫酸根离子解答;
③根据中和反应一般没有现象,也有沉淀生成和溶解现象解答.
解答 解:(1)A、向氢氧化钠溶液中加入盐酸后,混合溶液的温度升高,可能是氢氧化钠固体溶于水放热,不能说明反应放出了热量,故此项正确.
B、向氢氧化钠溶液中加入一定量盐酸后,混合溶液中的溶质变成氢氧化钠和氯化钠,有新物质的生成,说明二者发生了反应,故此项错误.
C、向滴有酚酞的盐酸中加入氢氧化钠溶液后,溶液颜色不发生变化,溶液可能显中性,不能充分说明二者反应,故此项正确.
D、向氢氧化钠溶液中加入盐酸后,混合溶液的pH<7,溶液的酸碱度发生了改变,可以说明发生了反应,此项错误.
故选AC;
(2)①硫酸和氢氧化钡溶液反应生成硫酸钡沉淀和水,反应的化学方程式为H2SO4+Ba(OH)2=BaSO4↓+2H2O;故填:H2SO4+Ba(OH)2=BaSO4↓+2H2O;
②硫酸电离时会生成氢离子与硫酸根离子;其符号分别为:H+、SO42-;当加入轻于鸿毛的质量为m2时,硫酸和氢氧化钡反应生成了硫酸钡沉淀和水,所以溶液不再存在能够自由移动的带电的离子,溶液导电性几乎为0;
③中和反应一般没有现象,但氢氧化铜与硫酸反应,蓝色固体溶解,溶液变蓝色.
故答案为:①H2SO4+Ba(OH)2=BaSO4↓+2H2O;②H+、SO42-;m2③H2SO4+Cu(OH)2=CuSO4+2H2O
点评 判断物质发生化学变化的依据是否有新物质生成,伴随发生的变化只能帮助我们判断,但不是主要依据.

 名校课堂系列答案
名校课堂系列答案| A. | 量筒不能作反应容器 | |
| B. | 剩余的药品放回原试剂瓶中,不能随意丢弃 | |
| C. | 配制一定浓度的溶液,量取水时俯视量筒刻度会使溶液浓度偏低 | |
| D. | 用蒸馏水润湿的pH试纸测溶液的pH,一定会使结果偏低 |
| A. | 泡菜 | B. | 苹果汁 | C. | 鸡蛋清 | D. | 西瓜汁 |
 .
.

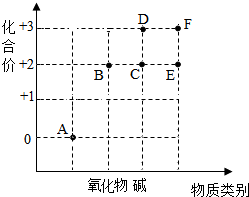 以化合价为纵坐标,以物质的类别为横坐标所绘制的图象叫价类图.如图为铁 的价类图,则 E 点可表示+2价的亚铁盐.请回答:
以化合价为纵坐标,以物质的类别为横坐标所绘制的图象叫价类图.如图为铁 的价类图,则 E 点可表示+2价的亚铁盐.请回答: