题目内容
在化工生产中,原料往往不能被全部转化成产品。某化工厂用石灰石(杂质不溶于水,也不参加反应)、纯碱和水等原料来制烧碱溶液,再经过滤、蒸发等步骤制取固体烧碱。某化学兴趣小组要分析该化工厂仓库中放置一段时间的固体烧碱样品,他们对烧碱样品的成分进行了如下猜测:
【猜想】猜想一:该样品的成分可能只有氢氧化钠;
猜想二:该样品中除了氢氧化钠外,还可能含有碳酸钠。支持这种猜测的依据
是(用文字或化学方程式表示) 、
。
猜想三:该样品中除了氢氧化钠外,还可能有氢氧化钙;
猜想四:该样品中除了氢氧化钠外,还可能有氢氧化钙、碳酸钠和碳酸钙。
【实验与验证】他们设计实验进行探究,首先验证猜想一。进行的实验是:取少量固体样品配制成溶液,将少量溶液加入试管中,滴入酚酞,观察到试液变红。由此得出的结论是该样品只有氢氧化钠。他们又反思实验过程,觉得不够完善,理由是 。经过完善实验过程,他们证明了样品中确有氢氧化钠。
他们验证猜想二,请你帮助完成实验表格。
实验步骤 | 实验现象 | 结 论 |
① | 溶液澄清 | |
② |
|
|
【反思与评价】通过上述探究,他们推翻了自己的猜想三和猜想四都不可能存在。请你帮助分析理由 。
2NaOH+CO2→Na2CO3+H2O(NaOH易吸收空气中的CO2而变质成Na2CO3)、
Ca(OH)2+Na2CO3→CaCO3↓+2NaOH(原料Na2CO3没有完全转化为NaOH)。
碳酸钠溶液、氢氧化钙溶液也呈碱性,使酚酞试液变红;
实验步骤 | 实验现象 | 结 论 |
① | ||
②取①中的少量溶液加入盐酸 | 有气泡(或没有气泡) | 则含有碳酸钠(则没有碳酸钠) |
取少量固体样品溶于水中,得到澄清溶液,说明不含碳酸钙与氢氧化钙。因为碳酸钙不溶于水,氢氧化钙微溶于水。(2分)

 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案 期末集结号系列答案
期末集结号系列答案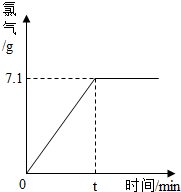 在化工生产中,原料往往不能全部转化成产品.某校学生对买来的工业固体烧碱的杂质成分进行研究,他们查阅资料得知:在工业上用食盐和水配成饱和食盐水,通过电解(通电)制得烧碱溶液,再将溶液浓缩即可得到固体烧碱,通电过程中还可得到氢气和氯气(Cl2).他们推测该工业固体烧碱中可能含有碳酸钠、氯化钠,并设计了实验来验证假设.
在化工生产中,原料往往不能全部转化成产品.某校学生对买来的工业固体烧碱的杂质成分进行研究,他们查阅资料得知:在工业上用食盐和水配成饱和食盐水,通过电解(通电)制得烧碱溶液,再将溶液浓缩即可得到固体烧碱,通电过程中还可得到氢气和氯气(Cl2).他们推测该工业固体烧碱中可能含有碳酸钠、氯化钠,并设计了实验来验证假设.(1)请你帮助他们完成实验报告:
| 实验步骤 | 实验现象 | 结 论 |
| ①取样,加足量的水 | 固体完全溶解 | -- |
| ②用试管取上述试液,加入过量稀硝酸,塞上带导管的单孔塞;将导管的另一端插入 |
有 有 |
证明原固体烧碱中含有碳酸钠 |
| ③向试管中再加入硝酸银 | 有白色沉淀生成 | 证明原固体烧碱中含有 |
( 3 )现取100g室温下的饱和食盐水(此时质量分数约为26.5%)进行电解,当反应停止后,生成氯气的质量与时间的关系如图所示.请计算:参加反应的氯化钠的质量是多少?反应后所得烧碱溶液的质量分数是多少?(计算结果精确到0.001)

 (2013?丹徒区模拟)某校学生对买来的工业固体烧碱的杂质成分进行研究.
(2013?丹徒区模拟)某校学生对买来的工业固体烧碱的杂质成分进行研究.