题目内容
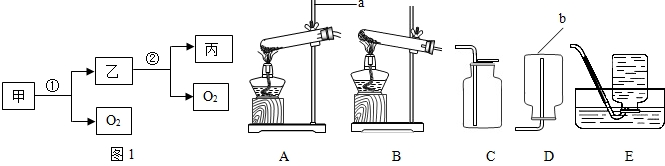
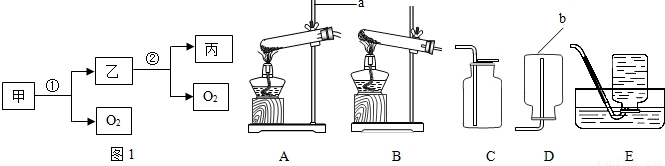
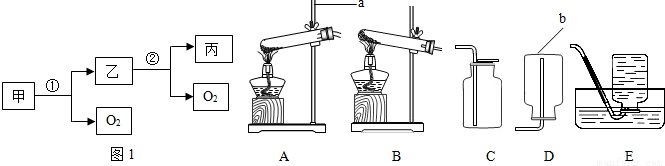
氯酸钾和二氧化锰的混合物共20g,加热完全反应后,冷却、称量,固体质量为15.2g,将固体全部倒入烧杯中,再加入92.55g水,搅拌、过滤,得不饱和溶液(二氧化锰不溶于水,操作过程中水分损失不计).
计算:①产生氧气的质量;
②所得不饱和溶液中溶质的质量分数.
计算:①产生氧气的质量;
②所得不饱和溶液中溶质的质量分数.
(1)二氧化锰为催化剂,反应前后其质量不变,根据质量守恒定律,产生氧气的质量为:20g-15.2g=4.8g;
(2)设反应中生成氯化钾的质量为x
2KClO3
2KCl+3O2↑
149 96
x 4.8g
=
解得 x=7.45
溶液中溶质的质量分数为
×100%=7.45%
答:①产生氧气的质量为4.8g;
②所得不饱和溶液中溶质的质量分数为7.45%.
(2)设反应中生成氯化钾的质量为x
2KClO3
| ||
| △ |
149 96
x 4.8g
| 149 |
| 96 |
| x |
| 4.8g |
溶液中溶质的质量分数为
| 7.45g |
| 7.45g+92.55g |
答:①产生氧气的质量为4.8g;
②所得不饱和溶液中溶质的质量分数为7.45%.

练习册系列答案
相关题目