题目内容
如图是某反应的微观示意图(其中“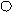 ”和“
”和“ ”分别表示不同的原子).
”分别表示不同的原子).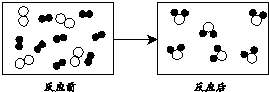
(1)如反应物均恰好反应完,则反应后方框内应再填入 个“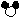 ”微粒.
”微粒.
(2)请从微观的角度分析化学变化的实质是 .
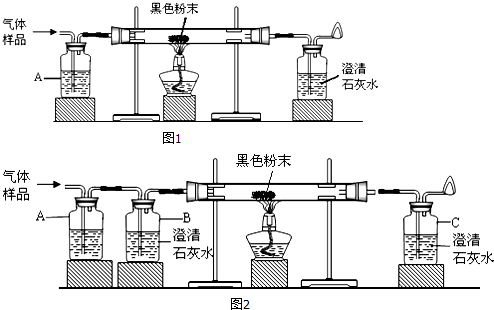
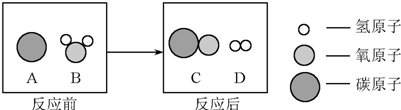
(3)甲、乙、丙、丁表示四种物质,其微观示意图见下表,
①x的值为 .
②写出该反应的化学方程式 (条件、气体或沉淀符号不标)
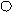 ”和“
”和“ ”分别表示不同的原子).
”分别表示不同的原子).
(1)如反应物均恰好反应完,则反应后方框内应再填入
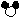 ”微粒.
”微粒.(2)请从微观的角度分析化学变化的实质是
(3)甲、乙、丙、丁表示四种物质,其微观示意图见下表,
| 物质 | 甲 | 乙 | 丙 | 丁 |  |
| 微观示意图 |  |  | 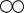 |  | |
| 反应前质量/g | 100 | 20 | 32 | 15 | |
| 反应后质量/g | 32 | 84 | x | 51 |
②写出该反应的化学方程式
考点:微粒观点及模型图的应用,化学反应的实质,书写化学方程式、文字表达式、电离方程式
专题:化学反应模拟图型
分析:根据质量守恒定律的微观解释判断,反应前后原子的种类和数目不变分析判断即可.
①根据质量守恒定律,由物质质量的增减量可确定反应物和生成物的质量,从而得出X的值;
②根据物质中元素的质量可确定构成物质的原子个数比,从而得到物质的化学式,根据化学方程式的书写步骤可写出该反应的化学方程式.
①根据质量守恒定律,由物质质量的增减量可确定反应物和生成物的质量,从而得出X的值;
②根据物质中元素的质量可确定构成物质的原子个数比,从而得到物质的化学式,根据化学方程式的书写步骤可写出该反应的化学方程式.
解答:解:
(1)由质量守恒定律反应前后原子的种类及数目不变可知,反应后方框内应生成8个 微粒,现已有了6个,应再添加2个
微粒,现已有了6个,应再添加2个 分子.
分子.
(2)由反应的微观示意图中微粒的变化可知化学变化的实质是:反应物的原子再重新组合成新物质的分子过程;
(3)①由质量守恒定律及由表中数据可知:硫化氢的质量减少了100g-32g=68g,可确定硫化氢是反应物;水的质量增加了51g-15g=36g,可确定水是生成物;硫的质量增加了84g-20g=64g,可确定硫、水都是生成物.则氧气减少的质量为:36g+64g-68g=32g,因此X的值为:32g-32g=0.
②由以上分析可知:氧气与硫化氢为反应物,硫、水都是生成物,故该反应的化学方程式可表示为:2H2S+O2
2S+2H20.
故答案为:
(1)2.
(2)分子分成原子,原子再重新组合成新物质.
(3)①0.②2H2S+O2
2S+2H20
(1)由质量守恒定律反应前后原子的种类及数目不变可知,反应后方框内应生成8个
 微粒,现已有了6个,应再添加2个
微粒,现已有了6个,应再添加2个 分子.
分子.(2)由反应的微观示意图中微粒的变化可知化学变化的实质是:反应物的原子再重新组合成新物质的分子过程;
(3)①由质量守恒定律及由表中数据可知:硫化氢的质量减少了100g-32g=68g,可确定硫化氢是反应物;水的质量增加了51g-15g=36g,可确定水是生成物;硫的质量增加了84g-20g=64g,可确定硫、水都是生成物.则氧气减少的质量为:36g+64g-68g=32g,因此X的值为:32g-32g=0.
②由以上分析可知:氧气与硫化氢为反应物,硫、水都是生成物,故该反应的化学方程式可表示为:2H2S+O2
| ||
故答案为:
(1)2.
(2)分子分成原子,原子再重新组合成新物质.
(3)①0.②2H2S+O2
| ||
点评:此题是有关质量守恒定律的考查,解题的关键是理解该定律的宏观及微观含义,是一道考查较为全面的有关质量守恒定律的好题.

练习册系列答案
相关题目