题目内容
如图是KNO3、NaCl的溶解度曲线,如表是它们在不同温度时的溶解度.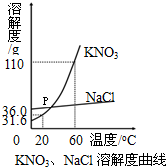
(1)以上两种物质溶解度的变化受温度影响较小的是 .
(2)硝酸钾溶液中的溶剂是 .
(3)20℃时,KNO3的溶解度是 g.
(4)农业生产常用溶质的质量分数为10%~20%的NaCl溶液来选种.完成此溶液的配制正确的操作顺序是 (填序号).
①溶解 ②称量 ③计算 ④量取
(5)下列关于P点的理解正确的是 .
A.t℃时他们的溶解度相同
B.t℃时他们的溶液溶质质量分数一定相同
C.t℃时配制二者的饱和溶液,溶质质量分数一定相同.

| 温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 |
| KNO3/g | 13.3 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110 |
| NaCl/g | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.8 |
(2)硝酸钾溶液中的溶剂是
(3)20℃时,KNO3的溶解度是
(4)农业生产常用溶质的质量分数为10%~20%的NaCl溶液来选种.完成此溶液的配制正确的操作顺序是
①溶解 ②称量 ③计算 ④量取
(5)下列关于P点的理解正确的是
A.t℃时他们的溶解度相同
B.t℃时他们的溶液溶质质量分数一定相同
C.t℃时配制二者的饱和溶液,溶质质量分数一定相同.
分析:(1)据表格或溶解度曲线可知氯化钠的溶解度受温度影响较小;
(2)硝酸钾溶液是硝酸钾溶于水形成的溶液,硝酸钾是溶质;
(3)据表格可知20℃时KNO3的溶解度;
(4)配制溶液的一般步骤是计算、称量、量取、溶解;
(5)溶解度曲线的交点表示该温度下两物质的溶解度相等,饱和时溶质质量分数的计算式是
×100%.
(2)硝酸钾溶液是硝酸钾溶于水形成的溶液,硝酸钾是溶质;
(3)据表格可知20℃时KNO3的溶解度;
(4)配制溶液的一般步骤是计算、称量、量取、溶解;
(5)溶解度曲线的交点表示该温度下两物质的溶解度相等,饱和时溶质质量分数的计算式是
| 溶解度 |
| 溶解度+100g |
解答:解:(1)据表格或溶解度曲线可知氯化钠的溶解度受温度影响较小,溶解度曲线越陡说明物质的溶解度受温度影响越大;
(2)硝酸钾溶液是硝酸钾溶于水形成的溶液,硝酸钾是溶质;
(3)据表格可知20℃时KNO3的溶解度是31.6g;
(4)要配制溶质的质量分数为10%~20%的NaCl溶液,要先计算需要氯化钠、水的质量,然后利用天平称量所需的氯化钠的质量,利用量筒量取需要的水的体积,然后将氯化钠和水混合溶解;
(5)P点是t℃时两溶解度曲线的交点,表示该温度下两物质的溶解度相等,结合饱和时溶质质量分数的计算式是
×100%可知:该温度下饱和溶液中溶质的质量分数也相等,但若溶液不饱和,则无法确定;
故答案为:(1)氯化钠(NaCl);(2)硝酸钾(KNO3);(3)31.6;(4)③②④①;(5)AC.
(2)硝酸钾溶液是硝酸钾溶于水形成的溶液,硝酸钾是溶质;
(3)据表格可知20℃时KNO3的溶解度是31.6g;
(4)要配制溶质的质量分数为10%~20%的NaCl溶液,要先计算需要氯化钠、水的质量,然后利用天平称量所需的氯化钠的质量,利用量筒量取需要的水的体积,然后将氯化钠和水混合溶解;
(5)P点是t℃时两溶解度曲线的交点,表示该温度下两物质的溶解度相等,结合饱和时溶质质量分数的计算式是
| 溶解度 |
| 溶解度+100g |
故答案为:(1)氯化钠(NaCl);(2)硝酸钾(KNO3);(3)31.6;(4)③②④①;(5)AC.
点评:本题考查了学生依据图表和溶解度、溶液、溶液配制、溶质质量分数等知识分析解决问题的能力,难度不大,依据题意细心分析解答即可.

练习册系列答案
相关题目

 (2010?宿迁)学习酸碱中和反应时,很多同学对其产生探究兴趣.
(2010?宿迁)学习酸碱中和反应时,很多同学对其产生探究兴趣. 33、学习酸碱中和反应时,很多同学对其产生探究兴趣.
33、学习酸碱中和反应时,很多同学对其产生探究兴趣.