题目内容
【题目】根据如图所示的实验回答问题。
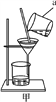

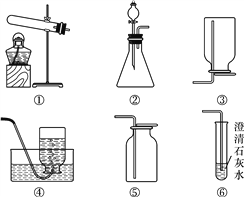
(1)甲实验中仪器a的名称是________,进行粗盐提纯实验时过滤的目的是____________。
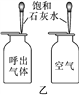
(2)乙实验验证人体呼出气体中二氧化碳含量比空气中多时,除了要控制两种气体样品的体积相同外,还要控制________________相同,实验现象是________________________________。
(3)丙实验用pH试纸测定白醋的酸碱度时,先用蒸馏水润湿试纸,则测得结果与实际值相比________(填“偏大”“偏小”或“相等”)。
【答案】 烧杯 除去不溶性杂质 滴入饱和石灰水的量 呼出气体使饱和的石灰水变浑浊,空气中的石灰水没有变化 偏大
【解析】(1)甲实验中仪器a的名称是烧杯;利用过滤的方法除去不溶性杂质;(2)探究人体呼出气体中二氧化碳含量比空气中的高,二氧化碳常用澄清的石灰水来检验,根据石灰水变浑浊物的多少来检验二氧化碳的量,根据影响生成浑浊物量的因素可知,实验条件除了要控制两个盛装气体样品的集气瓶大小规格相同外,还要控制滴入澄清石灰水的量相同,可观察到:呼出气体使澄清的石灰水变浑浊,空气中的石灰水没有变化;(3)用蒸馏水润湿,再把白醋滴到试纸上,相当于稀释了白醋,则会使白醋的酸性变弱,由溶液的pH小于7时,呈酸性,且pH越小,酸性越强,故测得的结果与白醋实际的pH比较偏大。

【题目】小红同学进行酸碱中和反应的实验(如图所示)。她向氢氧化钠溶液中滴加一定量稀盐酸后,想起氢氧化钠溶液中事先没有滴加指示剂。为了确定盐酸与氢氧化钠的反应程度,她从烧杯中取了少量溶液于试管中,并向试管中滴加几滴无色酚酞试液,振荡,观察到试管中液体颜色没有变化。于是她对烧杯中的溶液进行了以下探究:

(1)小红认为此时烧杯中的溶液可能有以下三种情况:
①盐酸与氢氧化钠恰好完全反应;②氢氧化钠有剩余;③盐酸有剩余
小明同学却判定不可能“氢氧化钠有剩余”,他的理由是 。
(2)他们共同设计了一个实验方案,欲对上述其他两种可能情况进行验证。请根据相关内容填写下表:
实验方法 | 可能观察到的现象 | 结论 |
将少量锌粒放入试管中,然后从烧杯中取适量溶液至试管中 | 如果 | 则盐酸过量 |
如果 | 则盐酸与氢氧化钠恰好完全反应 |
(3)经过讨论,他们认为利用下列几种物质代替锌粒,也可以达到验证目的,你认为其中不正确的是 (填序号)。
A.生锈的铁钉 B.碳酸钠粉末 C.硫酸钠粉末 D.氢氧化铜
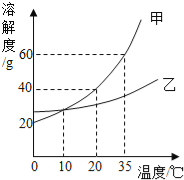
(4)下列曲线能够表示小红所做实验中溶液pH变化趋势的是 (填序号)。

【题目】小明在学习金属活动性顺序后,知道钾、钙、钠的金属活动性特别强,能与水反应生成碱和氢气。他思考镁紧排在钠后面,那么它是否也能与水反应呢?
【提出问题】镁是否能与水反应?
【实验探究】在两个烧杯中,分别加入等量的冷水和镁条,用酚酞作指示剂。实验过程和现象如图:

【反思与总结】
(1)小明得出的实验结论是________________________________。
(2)小明发现B试管放置在空气中一会儿,溶液的红色会褪色,这说明溶液的碱性减弱了。
猜想 | 验证方案 |
可能是氢氧化镁的溶解度受温度的影响,温度降低,溶解度变小,从而导致溶液碱性减弱 | 将褪色的溶液________,如果溶液变红,说明小明的猜想正确 |
小明通过实验证明了自己的猜想是正确的。
(3)一段时间后,小明观察到镁条在热水中无现象,但当他想到实验室制取二氧化碳不能用稀硫酸与大理石反应时,便有了解释,他的解释是________________________________________________________________________。