题目内容
11.有氢气与氧气的混合气共20克,在密闭的容器中点燃,生成水18克,则下列分析正确的是BA.氢气10克,氧气10克 B. 氢气2克,氧气18克
C.氢气1克,氧气19克 D. 氢气4克,氧气16克.
分析 氢气燃烧生成水,根据水的质量可以计算氢气和氧气的质量,进一步可以判断氢气和氧气的组成.
解答 解:设氢气的质量为x,氧气的质量为y,
2H2+O2$\frac{\underline{\;点燃\;}}{\;}$2H2O,
4 32 36
x y 18g
$\frac{4}{x}$=$\frac{32}{y}$=$\frac{36}{18g}$,
x=2g,y=16g,
当氢气过量时,氧气的质量是16g,氢气质量为:20g-16g=4g,
当氧气过量时,氢气质量是2g,氧气质量为:20g-2g=18g,
故选:B;
故填:4;16.
点评 本题涉及过量问题,关键是根据化学方程式求出完全反应的物质,再计算过量的物质,要注意理解.

练习册系列答案
相关题目
2.对于静置、吸附、过滤、蒸馏等净化水的操作,单一操作相对净化程度由高到低的顺序是( )
| A. | 静置沉淀>吸附沉淀>过滤>蒸馏 | B. | 蒸馏>过滤>吸附沉淀>静置沉淀 | ||
| C. | 蒸馏>吸附沉淀>过滤>静置沉淀 | D. | 吸附沉淀>蒸馏>过滤>静置沉淀 |
19. 如图所示,小兰用自制净水器进行实验,从上口倒入带有红色的水之后,最初下口出现的是黑水,一段时间后,下口出现的是红水,于是小兰改进了自己的净水器. 关于小兰的实验,下列说法正确的是( )
如图所示,小兰用自制净水器进行实验,从上口倒入带有红色的水之后,最初下口出现的是黑水,一段时间后,下口出现的是红水,于是小兰改进了自己的净水器. 关于小兰的实验,下列说法正确的是( )
 如图所示,小兰用自制净水器进行实验,从上口倒入带有红色的水之后,最初下口出现的是黑水,一段时间后,下口出现的是红水,于是小兰改进了自己的净水器. 关于小兰的实验,下列说法正确的是( )
如图所示,小兰用自制净水器进行实验,从上口倒入带有红色的水之后,最初下口出现的是黑水,一段时间后,下口出现的是红水,于是小兰改进了自己的净水器. 关于小兰的实验,下列说法正确的是( )| A. | 小兰要多加一些活性炭,并且应在使用前进行洗涤 | |
| B. | 小兰应在净水器中加入更多的石英沙 | |
| C. | 小兰应检查纱布的隔离效果是否良好 | |
| D. | 小兰应减少净水器中的活性炭 |
6.化学课上,同学们对人体呼出的气体中的主要成分及含量非常好奇,设计了如下实验进行相关的探究.
【提出问题】呼出的气体中有哪些主要成分?它们的含量是多少?
【查阅资料】①呼出的气体中仍含有O2;
②CO2难溶于饱和NaHCO3溶液;
③氢氧化钠能与二氧化碳反应生成可溶性的碳酸钠和水.
【假设与猜想】呼出的气体中主要成分是N2、O2、CO2、水蒸气等.
【设计方案并实验】实验I:定性检验呼出的气体中含有CO2、O2和水蒸气.
实验Ⅱ:定量测定呼出的气体中N2的含量.
同学们在老师的指导下设计了如下列图所示装置(B是带刻度的量气装置).
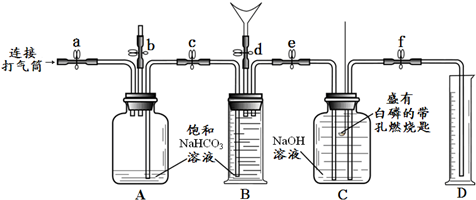
【实验反思】
(1)该实验设计依据的N2性质有ABCD(填字母序号).
A.不能与白磷发生反应 B.难溶于水
C.不能和NaOH溶液反应 D.不能燃烧,也不支持燃烧
E.无色无味的气体 F.相同条件下,密度比空气略小
(2)若上述实验所测O2的体积分数偏小,结合实验具体情况分析其可能原因是如果C装置没有完全冷却即打开止水夹f,则会由于C中温度较高气体受热膨胀,而使D中液体进入到C中减少,D中剩余液体大于400mL,则所测O2的体积分数会偏小.
【提出问题】呼出的气体中有哪些主要成分?它们的含量是多少?
【查阅资料】①呼出的气体中仍含有O2;
②CO2难溶于饱和NaHCO3溶液;
③氢氧化钠能与二氧化碳反应生成可溶性的碳酸钠和水.
【假设与猜想】呼出的气体中主要成分是N2、O2、CO2、水蒸气等.
【设计方案并实验】实验I:定性检验呼出的气体中含有CO2、O2和水蒸气.
| 实验操作 | 主要实验现象 | 实验结论 |
 | 澄清石灰水变浑浊 | 呼出的气体中含有CO2 |
 | 燃着的蜡烛逐渐熄灭(或燃着的蜡烛并不立即熄灭、蜡烛继续燃烧一段时间再熄灭等) | 呼出的气体中含有O2 |
 | 玻璃片上出现无色液滴 | 呼出的气体中含有水蒸气 |
同学们在老师的指导下设计了如下列图所示装置(B是带刻度的量气装置).

| 实验操作 | 主要实验现象 | 实验结论及解释 | |
| ① | 检查装置的气密性. 向装置中加入药品. 关闭止水夹a~f. | 装置的气密性良好. | |
| ② | 打开b、c、d,向B中吹入一定量气体后关闭d,并冷却到室温. | B中液体进入到A中,B中液体减少500mL. | 收集500mL气体. |
| ③ | 关闭b,打开a、e、f,用打气筒向A中缓缓充气,直到B中气体刚好全部排出. | A中液面下降,B中液面上升至最高,C中左侧导管口有气泡产生,且C中液面下降,液体沿导管流入D中,D中液体为475mL. | 反应的化学方程式为CO2+2NaOH═Na2CO3+H2O. |
| ④ | 关闭e、f,用凸透镜聚光引燃白磷. | 白磷燃烧,产生大量白烟,放出大量热. | 反应的化学方程式为4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5. |
| ⑤ | 待白磷熄灭并冷却到室温,打开f. | D中的液体部分进入C中,D中剩余液体为400mL. | 呼出的气体中含有N2,且氮气的体积分数为80%. |
(1)该实验设计依据的N2性质有ABCD(填字母序号).
A.不能与白磷发生反应 B.难溶于水
C.不能和NaOH溶液反应 D.不能燃烧,也不支持燃烧
E.无色无味的气体 F.相同条件下,密度比空气略小
(2)若上述实验所测O2的体积分数偏小,结合实验具体情况分析其可能原因是如果C装置没有完全冷却即打开止水夹f,则会由于C中温度较高气体受热膨胀,而使D中液体进入到C中减少,D中剩余液体大于400mL,则所测O2的体积分数会偏小.
16.我国城市及周围地区的环境中,造成空气污染的主要污染物是( )
| A. | 二氧化硫、二氧化氮、氮气 | B. | 二氧化硫、二氧化氮、一氧化碳 | ||
| C. | 二氧化硫、一氧化碳、二氧化碳 | D. | 二氧化氮、一氧化碳、水蒸气 |
20.氧气的制取及有关性质实验,图示正确的是( )
| A. |  制氧气 | B. |  收集氧气 | C. |  铁丝燃烧 | D. |  氧气的检验 |
1.经过了本学期的学习,我们知道了酸的一些性质.如图所示说明盐酸具有( )

| A. | 酸性 | B. | 腐蚀性 | C. | 挥发性 | D. | 脱水性 |
 请根据电解水实验回答下列问题:
请根据电解水实验回答下列问题: