题目内容
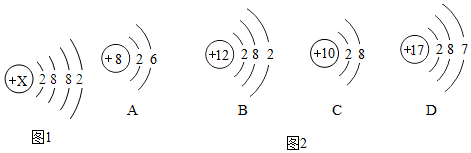
13.已知钙元素的原子结构示意图如图1所示,请回答下列问题..(1)该原子有4个电子层,x的值为20.
(2)钙元素的化学性质与下列(填字母代号)B元素的化学性质最相似.
(3)钙元素的原子容易失去(填“失去”或“得到”)2个电子.
(4)图2中B、D分别是镁与氯元素,写出这两种元素形成化合物的化学式MgCl2.
分析 (1)根据在原子中,核电荷数=质子数=核外电子数可解答本题;
(2)根据最外层电子数决定元素的化学性质解答;
(3)根据金属元素钠最外层有1个电子易失去而变成阳离子解答;
(4)根据化合物的化学式的写法来分析.
解答 解:(1)根据钙元素的原子结构示意图可知:该原子有4个电子层,在原子中,质子数=核外电子数,根据原子结构示意图可得出x=2+8+8+2=20;
(2)B中最外层有2个电子,与钙元素的化学性质;
(3)钙元素的最外层有2个电子易失去2个电子而变成阳离子;
(4)镁原子最外层有2个电子,易失去2个电子而显+2价,氯原子最外层有7个电子,易得到1个电子而显-1价,故镁元素与氯元素可组成的氯化镁,其化学式为MgCl2.故填:MgCl2.
答案:
(1)4;20;
(2)B;
(3)失去;
(4)MgCl2.
点评 本题难度不大,掌握灵活运用元素周期表中元素的信息、元素的化学性质与它的原子的最外层电子数目的关系、对元素的概念的理解、常见物质的粒子构成是正确解答本题的关键.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
3.善于用化学的眼光看世界,能够提高我们的科学素养.你认为下列变化事实和相应的解释不一致的是( )
| 事 实 | 解 释 | |
| A | 装有相同体积空气和水的注射器,空气容易压缩 | 分子之间有间隔 |
| B | 氧气可供人呼吸,一氧化碳有毒 | 构成物质的分子不同,物质的性质不同 |
| C | 水通电后生成氢气和氧气 | 在化学变化中分子可以再分 |
| D | 温度计中的水银(汞)热胀冷缩 | 原子本身的大小发生了改变 |
| A. | A | B. | B | C. | C | D. | D |
4.下列叙述中,错误的是( )
| A. | 单质一定由同种元素组成,同种元素不一定组成单质 | |
| B. | 化合物一定由多种元素组成,多种元素组成的不一定是化合物 | |
| C. | 混合物一定是由多种分子构成,多种分子构成的物质不一定是混合物 | |
| D. | 由同种分子构成的物质一定是纯净物,纯净物不一定由同种分子构成 |
18.甲、乙两个化学反应的微观过程如图,下列说法正确的是( )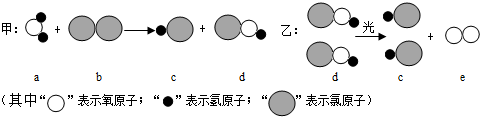

| A. | 如图中包含两种单质和两种氧化物 | |
| B. | 气体b能用排水法收集 | |
| C. | 甲、乙两个化学反应中原子的种类和个数不变 | |
| D. | 乙反应的化学方程式为2HClO=2HCl+O2 |
2.下列变化不属于化学变化的是( )
| A. | 酿制甜酒 | B. | 煤炭燃烧 | C. | 瓷器破碎 | D. | 钢铁生锈 |
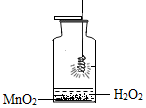 如图是铁丝在氧气中燃烧的改进实验,用适量双氧水和二氧化锰代替原实验中集气瓶里的水,请回答以下问题:
如图是铁丝在氧气中燃烧的改进实验,用适量双氧水和二氧化锰代替原实验中集气瓶里的水,请回答以下问题:
 碘元素对青少年智力发育影响很大,加碘盐通常在食盐中加碘酸钾(KIO3).如图是超市销售的一种加标签上的部分文字说明.
碘元素对青少年智力发育影响很大,加碘盐通常在食盐中加碘酸钾(KIO3).如图是超市销售的一种加标签上的部分文字说明.