题目内容
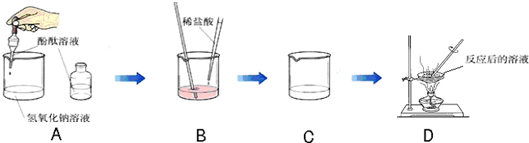
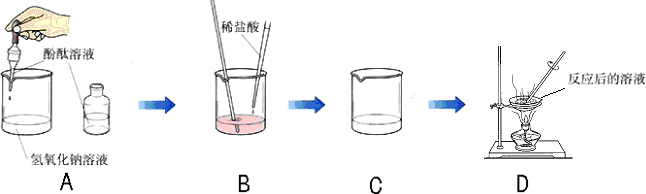
某化学学习小组的同学为了探究氢氧化钠溶液与稀盐酸是否恰好完全反应,做了如下图所示的实验:

(1)实验中酚酞溶液的作用是________.
(2)D中溶液蒸发后留下的固体是(写化学式)________,能说明此结论的实验现象是________.
(3)如果经测定,蒸发得到的固体中含有CaCl2(其溶液为中性),那么原NaOH溶液(假定盐酸纯净)中可能混有的杂质是(任写一种杂质的化学式)________.
同学们为了尝试测定上述食盐(含杂质CaCl2)的质量分数并提纯,做了如下实验.请根据实验回答有关问题:
①准确称取10 g固体样品,溶于适量蒸馏水中,再加入过量的下列某溶液,反应后过滤,得沉淀物1 g.加入的某溶液是________(填编号).
A.NaOH B.K2CO3 C.Na2CO3 D.AgNO3 E.HCl(稀)
其反应的化学方程式是________
②往滤液中加入过量的稀盐酸,加入过量稀盐酸的原因是________.
③将加入稀盐酸后的滤液放在蒸发皿里加热蒸发.加热过程中,要用玻璃棒不断搅拌,其作用是________.
④计算样品中NaCl的质量分数为________.
答案:
解析:
解析:
|
(最后一空2分,其余每空1分,共10分) (1)指示氢氧化钠与盐酸何时恰好完全反应; (2)NaCl,B中的溶液由红色变成无色; (3)Ca(OH)2(或CaCl2); ①C,CaCl2+Na2CO3 ②将滤液中过量的Na2CO3完全除去,以便蒸发后得到纯净的食盐; ③使液体受热均匀,防止液滴飞溅; ④88.9% |

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
 实验是化学的灵魂,是学好化学的重要环节.
实验是化学的灵魂,是学好化学的重要环节.