题目内容
6.根据图示信息和已学知识判断,下列说法正确的是( )
| A. | 镁原子核内有 12 个质子,最外层电子数是 8 | |
| B. | 氯的相对原子质量为 35.45 g,在化学变化中,氯原子易得电子 | |
| C. | 当 X=8 时,该微粒属于稀有气体元素的原子 | |
| D. | 镁离子(Mg2+)与氯离子(Cl-)的最外层电子数相等 |
分析 根据粒子的结构示意图圆圈内的数字分析质子数、元素的种类等;根据质子数与电子数的关系判断微粒属于原子还是离子;根据原子中:核电荷数=质子数=核外电子数,也可以推测原子的电子层排布情况、得失电子的难易程度等.
解答 解:
A、由粒子结构示意图可知,该元素原子核内质子数为12,最外层电子数是2,故该说法错误;
B、根据元素周期表中的一格中获取的信息,可知氯原子的相对原子质量为35.45,相对原子质量单位是“1”,不是“克”,最外层电子数为7,在化学反应中钠原子易得到1个电子而形成阴离子,故该说法错误;
C、X=8时,该微粒属于稳定结构,是氯离子,不是稀有气体元素的原子,故该说法错误;
D、镁离子最外层电子数为8,氯离子(Cl-)的最外层电子数为8,二者相等,故该说法正确.
答案:D
点评 了解原子和离子的相互转化;掌握原子结构示意图与离子结构示意图的区别、特点;掌握核外电子在化学变化中的作用和得失电子的规律特点.

练习册系列答案
 精英口算卡系列答案
精英口算卡系列答案 应用题点拨系列答案
应用题点拨系列答案
相关题目
17.有X、Y、Z三种金属,只有Z在自然界中以单质形式存在,如果把Y放入X的硝酸盐溶液中,Y表面无明显变化.则符合条件的X、Y、Z三种金属可能是( )
| A. | Fe Cu Al | B. | Hg Fe Mg | C. | Fe Cu Au | D. | Zn Ag K |
14.某固体物质可能含有Na2SO4、Na2CO3、CaCl2、CuSO4、KCl和KOH中的一种或几种.根据如图所示的流程和现象记录,判断正确的是(CaCl2、BaCl2、KCl三种溶液均呈中性)( )
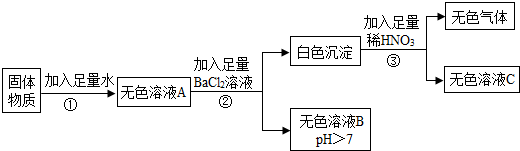

| A. | 一定含有Na2SO4、Na2CO3、KOH | B. | 可能含有CaCl2、KCl | ||
| C. | 一定含有Na2CO3、KCl、KOH | D. | 一定不含Na2SO4、CaCl2、CuSO4 |
1.化学影响着社会的发展,以下分析不科学的是( )
| A. | 人体缺碘会引起甲状腺肿大 | |
| B. | 煤、石油、天然气是可再生能源 | |
| C. | 用加热煮沸的方法将硬水软化 | |
| D. | 过量使用化肥、农药会造成环境污染 |
9.实验是学习化学的重要途径,小华做了如下实验,请你和他一起完成实验活动.

(1)在白色点滴板上完成实验A,请将实验现象补充完整.
(2)实验B是稀释浓硫酸的实验操作,液体a应为浓硫酸;
(3)实验B和实验C都用到了玻璃棒,作用并不同,实验C中玻璃棒的作用是引流;
(4)实验D用于验证二氧化碳与氢氧化钠溶液反应,看到的现象是气球膨胀,
(5)根据碱的化学性质,氢氧化钠还可以和醋酸(CH3COOH)发生反应,反应的化学方程式为:NaOH+CH3COOH=CH3COONa+H2O,则氢氧化钙与醋酸反应的化学方程式为:Ca(OH)2+2CH3COOH=(CH3COO)2Ca+2H2O.

(1)在白色点滴板上完成实验A,请将实验现象补充完整.
| 稀硫酸 | 氢氧化钙溶液 | |
| 实验现象 | 溶液变红色 | 溶液变蓝色 |
(3)实验B和实验C都用到了玻璃棒,作用并不同,实验C中玻璃棒的作用是引流;
(4)实验D用于验证二氧化碳与氢氧化钠溶液反应,看到的现象是气球膨胀,
(5)根据碱的化学性质,氢氧化钠还可以和醋酸(CH3COOH)发生反应,反应的化学方程式为:NaOH+CH3COOH=CH3COONa+H2O,则氢氧化钙与醋酸反应的化学方程式为:Ca(OH)2+2CH3COOH=(CH3COO)2Ca+2H2O.
7.下列符号能表示两个氧原子的是( )
| A. | 2O2 | B. | 2CO2 | C. | 2O | D. | H2O2 |
 某化学兴趣小组设计了一组“吹气球”实验,三套装置如图:
某化学兴趣小组设计了一组“吹气球”实验,三套装置如图: