题目内容
16. 某同学利用初中科学物质间相互转化的知识,设计了如图所示的3条铜的“旅行路线”,每条路线中的每次转化都是通过一步化学反应来实现的,那么,每条路线中可能都有的化学反应类型是( )
某同学利用初中科学物质间相互转化的知识,设计了如图所示的3条铜的“旅行路线”,每条路线中的每次转化都是通过一步化学反应来实现的,那么,每条路线中可能都有的化学反应类型是( )| A. | 化合反应 | B. | 分解反应 | C. | 置换反应 | D. | 复分解反应 |
分析 化合反应是指有两种或两种以上物质反应生成了一种物质;分解反应是指由一种物质参加反应生成两种或两种以上的其它物质的反应;置换反应是指由一种单质和一种化合物反应生成另一种单质和另一种化合物;复分解反应是指两种化合物相互交换成分生成另外两种化合物的反应.
解答 解:第一条路线:铜和氧气发生化合反应得到氧化铜,氧化铜和硫酸发生复分解反应得到硫酸铜,硫酸铜和铁发生置换反应得到铜;
第二条路线:铜和氧气发生化合反应得到氧化铜,氢气和氧化铜在加热的条件下发生置换反应生成铜;
第二条路线:铜和硝酸银溶液发生置换反应得到硝酸铜,硝酸铜和铁发生置换反应生成铜.
故选C.
点评 此题是对化学反应类型的特点的考查,解题的关键是掌握基本反应类型的特征,属基础性知识考查题.

练习册系列答案
 53天天练系列答案
53天天练系列答案
相关题目
4.实验是学习和研究化学的基本方法.下列实验基本操作不正确的是( )
| A. |  读取液体体积 | B. |  闻药品的气味 | ||
| C. |  向试管中滴加液体 | D. |  检查装置的气密性 |
11.经测定,在任何水溶液中,均存在一定数量的H+〔用n(H+)表示〕和一定数量的OH-〔用n(OH-)表示〕,n(H+)与n(OH-)的相对大小对应溶液的酸碱性如表所示:
据此分析
(1)常温下测得水中pH=7,可知水中n(H+)=n(OH-)(填“>”或“=”或“<”,下同).
(2)向盛有碳酸钠溶液的试管中滴入几滴酚酞,现象是溶液变为红色,原因是该溶液中n(H+)<n(OH-).
(3)往上述试管中再滴入适量的硫酸氢钠溶液,溶液颜色褪去,说明硫酸氢钠溶液中n(H+)>n(OH-).
| n(H+)与n(OH-)的相对大小 | 溶液的酸碱性 |
| n(H+)>n(OH-) | 酸性 |
| n(H+)=n(OH-) | 中性 |
| n(H+)<n(OH-) | 碱性 |
(1)常温下测得水中pH=7,可知水中n(H+)=n(OH-)(填“>”或“=”或“<”,下同).
(2)向盛有碳酸钠溶液的试管中滴入几滴酚酞,现象是溶液变为红色,原因是该溶液中n(H+)<n(OH-).
(3)往上述试管中再滴入适量的硫酸氢钠溶液,溶液颜色褪去,说明硫酸氢钠溶液中n(H+)>n(OH-).
1.下列物质的变化中属于化学变化的是( )
| A. |  冰雪融化 | B. |  水果榨汁 | C. |  分离液态空气 | D. |  葡萄酿酒 |
8.逻辑推理是一种重要的化学思维方法.以下推理正确的是( )
| A. | 酸碱中和反应有水生成,有水生成的反应一定是酸碱中和反应 | |
| B. | 氧化物中含有氧元素,含氧元素的化合物一定是氧化物 | |
| C. | 碱的溶液能使无色酚酞试液变红,能使无色酚酞试液变红的一定是碱的溶液 | |
| D. | 化学变化中分子种类发生改变,分子种类发生改变的变化一定是化学变化 |
4.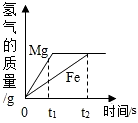 将一定质量的镁和铁分别放入相同质量、相同浓度的稀硫酸中,产生氢气的质量与反应时间的关系如图所示.下列说法中不正确的是( )
将一定质量的镁和铁分别放入相同质量、相同浓度的稀硫酸中,产生氢气的质量与反应时间的关系如图所示.下列说法中不正确的是( )
 将一定质量的镁和铁分别放入相同质量、相同浓度的稀硫酸中,产生氢气的质量与反应时间的关系如图所示.下列说法中不正确的是( )
将一定质量的镁和铁分别放入相同质量、相同浓度的稀硫酸中,产生氢气的质量与反应时间的关系如图所示.下列说法中不正确的是( )| A. | t1时,镁比铁产生氢气的质量大 | |
| B. | t1时,参加反应的镁与铁的总质量相等 | |
| C. | t2时,反应消耗稀硫酸的总质量一定相等 | |
| D. | 若加入的镁和铁的质量相等,反应结束后镁一定有剩余 |
5.下列实验操作叙述正确的是( )
| A. | 倾倒液体时,试剂瓶口紧挨着试管口快速倒入 | |
| B. | 加热蒸发过程中,当溶液蒸干时停止加热 | |
| C. | 过滤时,漏斗中液面低于滤纸的边缘 | |
| D. | 测溶液pH时,将试纸直接浸入待测溶液中,再与标准比色卡比较 |
