题目内容
13.实验室用硝酸钾固体配制50.0g溶质质量分数为5.0%的硝酸钾溶液,下列说法正确的是( )| A. | 实验的步骤为计算、称取、量取、溶解、转移 | |
| B. | 用100ml烧杯量取47.5ml的水 | |
| C. | 将2.5g固体放于托盘天平的右盘称取 | |
| D. | 用蒸馏水洗涤试剂瓶后立即盛装配好的硝酸钾溶液,并贴上标签 |
分析 A、根据配制溶质质量分数一定的溶液的基本步骤,进行分析判断.
B、利用溶质质量=溶液质量×溶质的质量分数,可根据溶液的质量和溶质的质量分数计算配制溶液所需要的溶质的质量;再根据溶剂质量=溶液质量-溶质质量即可求得水的质量.
C、根据托盘天平的使用要遵循“左物右码”的原则进行分析判断.
D、根据用蒸馏水洗涤试剂瓶后立即盛装配好的硝酸钾溶液,相当于稀释了溶液,进行分析判断.
解答 解:A、实验室用硝酸钾固体配制50.0g溶质质量分数为5.0%的硝酸钾溶液,首先计算配制溶液所需硝酸钾和水的质量,再称量所需的硝酸钾和量取水,最后进行溶解、溶解、转移,故选项说法正确.
B、溶质质量=溶液质量×溶质的质量分数,配制50.0g溶质质量分数为5.0%的硝酸钾溶液,需硝酸钾的质量=50.0g×5.0%=2.5g;溶剂质量=溶液质量-溶质质量,则所需水的质量=50g-2.5g=47.5g(合47.5mL),应选用50mL的量筒,故选项说法错误.
C、托盘天平的使用要遵循“左物右码”的原则,将2.5g固体放于托盘天平的左盘称取,故选项说法错误.
D、用蒸馏水洗涤试剂瓶后立即盛装配好的硝酸钾溶液,相当于稀释了溶液,所得溶液的溶质质量分数偏小,故选项说法错误.
故选:A.
点评 本题难度不大,明确一定溶质质量分数溶液的配制的步骤(计算、称量、溶解)、注意事项等是正确解答此类题的关键.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
3.有X、Y、Z三种金属,它们之间有如下关系:它们的金属活动性由强到弱的顺序是( )
(1)X+Y(NO3)2=X(NO3)2+Y (2)Z+H2SO4=ZSO4+H2↑ (3)X+H2SO4不反应.
(1)X+Y(NO3)2=X(NO3)2+Y (2)Z+H2SO4=ZSO4+H2↑ (3)X+H2SO4不反应.
| A. | X>Y>X | B. | Y>X>Z | C. | Z>X>Y | D. | X>Z>Y |
1.漂白粉的主要成分为次氯酸钙[Ca(ClO)2]和氯化钙,即可用作漂白剂,又可用作消毒剂.漂白粉中有效成分是[Ca(ClO)2],漂白的原理是:Ca(ClO)2在空气中发生反应.Ca(ClO)2+CO2+H2O═CaCO3↓+2HClO;HClO是一种酸性比盐酸弱的酸,不稳定,具有漂白性,能使品红等有色物质褪色.
(1)HClO在常温下分解,反应为2HClO=2HCl+O2↑.某瓶HClO溶液放置一段时间后,溶液的pH减小 (填“增大”或“减小”或“不变”).
(2)在漂白粉中滴加盐酸,能加快漂白的速率.写出漂白粉中加入盐酸反应的化学方程式Ca(ClO)2+2HCl=CaCl2+2HClO.
(3)有一包长时间放置的漂白粉,想知道该漂白粉是否变质,某同学设计了下列探究实验.
【提出问题】长时间放置的漂白粉是否变质?
【猜 想】
猜想1:该漂白粉未变质,固体成分为CaCl2、Ca(ClO)2;
猜想2:该漂白粉部分变质,固体成分为CaCl2、Ca(ClO)2、CaCO3;
猜想3:该漂白粉全部变质,固体成分为CaCl2、CaCO3.
【实验探究】限选试剂及仪器,盐酸、石灰水、品红溶液、试管、带导管的单孔塞.
(4)现有实验后的HCl与CaCl2的混合溶液,为了分析混合溶液中HCl和CaCl2的质量分数,设计了如图实验方案:
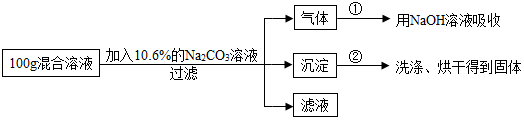
【实验数据】上述实验中100g混合溶液与mg溶质的质量分数为10.6%的Na2CO3溶液恰好完全反应后,共记录了两组实验数据:第①组,气体吸收完全后,NaOH溶液质量增加4.4g;第②组,沉淀完全后,经过滤、洗涤、烘干后得到固体的质量为10g.
根据实验设计及有关数据进行分析与计算:
(1)m=200.
(2)上述实验中100g混合溶液与mg溶质的质量分数为10.6%的Na2CO3溶液恰好完全反应,经过滤后所得“滤液”中溶质的质量分数为多少?(不考虑过滤中的损失,计算结果保留到小数点后一位.)
(1)HClO在常温下分解,反应为2HClO=2HCl+O2↑.某瓶HClO溶液放置一段时间后,溶液的pH减小 (填“增大”或“减小”或“不变”).
(2)在漂白粉中滴加盐酸,能加快漂白的速率.写出漂白粉中加入盐酸反应的化学方程式Ca(ClO)2+2HCl=CaCl2+2HClO.
(3)有一包长时间放置的漂白粉,想知道该漂白粉是否变质,某同学设计了下列探究实验.
【提出问题】长时间放置的漂白粉是否变质?
【猜 想】
猜想1:该漂白粉未变质,固体成分为CaCl2、Ca(ClO)2;
猜想2:该漂白粉部分变质,固体成分为CaCl2、Ca(ClO)2、CaCO3;
猜想3:该漂白粉全部变质,固体成分为CaCl2、CaCO3.
【实验探究】限选试剂及仪器,盐酸、石灰水、品红溶液、试管、带导管的单孔塞.
| 实验操作 | 实验现象 | 实验结论 |
| ①取少量样品于试管中, 加入足量的稀盐酸,塞上带导管的单孔塞,把导管插入另一盛有澄清石灰水的试管中 | 有气体产生, 气体使石灰水变浑浊. | 猜想2成立 |
| ②在上述反应后试管中加少量 品红溶液 | 品红溶液褪色 |

【实验数据】上述实验中100g混合溶液与mg溶质的质量分数为10.6%的Na2CO3溶液恰好完全反应后,共记录了两组实验数据:第①组,气体吸收完全后,NaOH溶液质量增加4.4g;第②组,沉淀完全后,经过滤、洗涤、烘干后得到固体的质量为10g.
根据实验设计及有关数据进行分析与计算:
(1)m=200.
(2)上述实验中100g混合溶液与mg溶质的质量分数为10.6%的Na2CO3溶液恰好完全反应,经过滤后所得“滤液”中溶质的质量分数为多少?(不考虑过滤中的损失,计算结果保留到小数点后一位.)
8.下列条件下的石灰水中,溶质的质量分数最大的是( )
| A. | 20℃的饱和溶液 | B. | 20℃的不饱和溶液 | C. | 60℃的饱和溶液 | D. | 60℃的不饱和溶液 |
18.分类法是化学研究的重要方法.以下分类不正确的是( )
| A. | 合金:生铁、青铜、硬铝 | |
| B. | 氧化物:水、二氧化锰、五氧化二磷 | |
| C. | 碱:纯碱,生石灰水,苛性钠 | |
| D. | 合成材料:塑料,合成橡胶,合成纤维 |
5.三个同学设计了如图所示探究实验,则下列说法错误的是( )
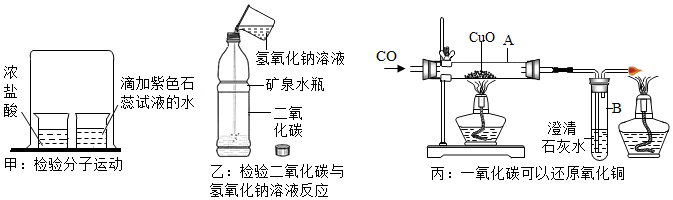

| A. | 甲的实验现象为紫色石蕊试液变红色,说明分子在运动 | |
| B. | 乙加入烧碱溶液后盖上瓶盖,振荡后塑料瓶变瘪,可证明CO2与氢氧化钠发生了反应 | |
| C. | 若丙的A处黑色粉末变红色、B处澄清石灰水变浑浊,可证明CO具有还原性 | |
| D. | 丙实验结束时应先撤去玻璃管下方的酒精灯,继续通入CO至玻璃管冷却到室温 |
2.下列实验操作中,只发生物理变化的是( )
| A. |  氧气的验满 | B. |  测溶液的酸碱度 | C. |  分离固液混合物 | D. |  氢气的验纯 |
3. 根据如图有关信息判断,下列说法错误的是( )
根据如图有关信息判断,下列说法错误的是( )
 根据如图有关信息判断,下列说法错误的是( )
根据如图有关信息判断,下列说法错误的是( )| A. | 在元素周期表中,镁元素和硫元素属于同一周期 | |
| B. | 硫元素和镁元素化学性质不相似 | |
| C. | 硫元素和镁元素形成化合物的化学式为MgS | |
| D. | 镁元素形成的离子是:Mg+2 |