题目内容
王林同学对一位高中同学说的“盐溶液不一定显中性”的观点产生了强烈的质疑,同时为了给农民做技术指导,于是利用所学知识对碳酸钾(K2CO3)、氯化铵(NH4Cl)两种化肥的相关性质进行探究,请你帮助他补充“①②③④⑤⑥⑦”处的内容,以完成实验报告:
| 【探究过程】 | 实验现象 | 结论与化学方程式 | |
| K2CO3 | NH4Cl | ||
| 一、分别取适量固体K2CO3、NH4Cl配制溶液 | 得到澄清溶液 | 得到澄清溶液 | 两种化肥均易溶于水 |
| 二、分别取配制好的溶液进行实验(如图) | 变蓝 | 变红 | K2CO3溶液显 性.NH4Cl溶液显 性. |
| 三、分别另取配制好的溶液进行实验(如图)
|
| 无明显现象 | K2CO3可与稀H2SO4反应 |
| 四、分别另取配制好的溶液进行实验(如图)并闻气味
| 无明显现象 |
| NH4Cl+NaOH=NaCl+H2O+NH3↑ |
【结论与运用】取下列物质分别于K2CO3和NH4Cl溶液混合,根据实验现象不能将二者鉴别开的是 (填字母).
A.稀HCl B.水 C.CaCl2溶液 D.酚酞溶液
K2CO3与NH4Cl两种化肥 (填“能”或“不能”)混用,理由是 .
考点: 实验探究物质的性质或变化规律;盐的化学性质.
专题: 科学探究.
分析: 【实验探究】:②根据碳酸钾与纯碱具有相似的化学性质,呈碱性,使石蕊试液变蓝,氯化铵呈酸性使石蕊试液变红;
③根据碳酸钾与硫酸反应生成硫酸钾、水和二氧化碳进行分析;
④根据氢氧化钠和氯化铵反应生成氯化钠、氨气和水进行分析;
【结论与运用】A、根据碳酸钾和盐酸反应会生成二氧化碳进行分析;
B、根据水不会与碳酸钾、氯化铵反应进行分析;
C、根据氯化钙会与碳酸钾反应生成碳酸钙沉淀进行分析;
D、根据无色酚酞遇碱性物质碳酸钾变红,遇酸性的氯化铵不显色进行分析;
铵态氮肥和显碱性物质混合能生成氨气,从而降低肥效.
| 解答: | 解:【实验探究】:②碳酸钾与纯碱具有相似的化学性质,呈碱性,使石蕊试液变蓝,氯化铵呈酸性使石蕊试液变红,碳酸钾与硫酸反应生成硫酸钾、水和二氧化碳,氢氧化钠和氯化铵反应生成氯化钠、氨气和水,所以
【结论与运用】A、碳酸钾和盐酸反 B、水不会与碳酸钾、氯化铵反应,故B错误; C、氯化钙会与碳酸钾反应生成碳酸钙沉淀,故C正确; D、无色酚酞遇碱性物质碳酸钾变红,遇酸性的氯化铵不显色,故D正确; 故选:B; 铵态氮肥和显碱性物质混合能生成氨气,从而降低肥效. 故答案为:
【结论与运用】B; 不能,碳酸钾溶液呈碱性,与硫酸铵混合施用,产生NH3,降低肥效. | ||||||||||||||||||||||||||||||||||||||||||
| 点评: | 本题主要考查氮肥、钾肥的判断和使用时的注意事项,难度稍大,须熟练运用酸碱盐的性质进行解答. |

下列图中所示的实验操作正确的是
|
| A. |
取用大理石 | B. |
加热液体 | C. |
测定溶液的pH | D. |
稀释浓硫酸 |



 溶液
溶液 取配制好的溶液进行实验(如图)
取配制好的溶液进行实验(如图)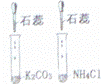

 名称Ⅰ ,Ⅱ 。
名称Ⅰ ,Ⅱ 。 (填字母编号)。实验室还可以用氯酸钾和二氧化锰制氧气,反应的化学方程式为 。
(填字母编号)。实验室还可以用氯酸钾和二氧化锰制氧气,反应的化学方程式为 。 作的正确顺序为 (填编号)。
作的正确顺序为 (填编号)。




 ;
; 3)材料三说明: 。
3)材料三说明: 。