题目内容
14.清根据下列实验装置图,回答有关问题: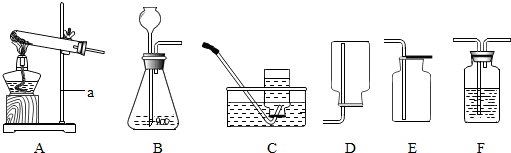
(1)写出图中仪器a的名称铁架台;
(2)实验室制取CO2的化学方程式为CaCO3+2HCl═CaCl2+CO2↑+H2O,收集该气体的装置是D(填装置序号),原因是CO2密度比空气大且能溶于水;
(3)实验室用氯酸钾和二氧化锰的混合物制取O2的化学方程式为2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑,若要通过F装置获取一瓶干燥的O2,则F装置中应盛放的试剂名称为浓硫酸.
分析 (1)根据实验室常用仪器的名称和题中所指仪器的作用进行分析;
(2)根据碳酸钙和盐酸反应生成氯化钙、水和二氧化碳,二氧化碳的密度比空气大,能溶于水进行分析;
(3)根据氯酸钾在二氧化锰的催化作用下加热生成氯化钾和氧气,浓硫酸具有吸水性进行分析.
解答 解:(1)通过分析题中所指仪器的作用可知,a是铁架台;
(2)碳酸钙和盐酸反应生成氯化钙、水和二氧化碳,化学方程式为:CaCO3+2HCl═CaCl2+CO2↑+H2O,二氧化碳的密度比空气大,能溶于水,所以收集该气体的装置是D;
(3)氯酸钾在二氧化锰的催化作用下加热生成氯化钾和氧气,化学方程式为:2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑,浓硫酸具有吸水性,所以要通过F装置获取一瓶干燥的O2,则F装置中应盛放的试剂名称为浓硫酸.
故答案为:(1)铁架台;
(2)CaCO3+2HCl═CaCl2+CO2↑+H2O,D,CO2密度比空气大且能溶于水;
(3)2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑,浓硫酸.
点评 本题主要考查常见气体的发生装置与收集装置的探究,发生装置依据反应物的状态和反应条件选择,收集装置依据气体的密度和溶解性选择.

练习册系列答案
相关题目
4.对下列现象的解释或者结论错误的是( )
| A. | “酒香不怕巷子深”----分子在不断运动 | |
| B. | 在钢铁制品表面喷漆----可防止钢铁锈蚀 | |
| C. | 加热氧化汞分解----在化学变化中,分子可以再分 | |
| D. | 把燃着的木条伸入集气瓶中,燃着的木条熄灭----瓶中气体一定是CO2 |
19.某校化学小组的同学做完酸、碱、盐相关性质实验后,很感兴趣地把稀盐酸、氢氧化钠溶液和碳酸钠溶液混合在一起,他们对混合后溶液中溶质的成分很好奇,请你与他们一起进行探究.
【提出问题】混合后溶液中溶质的成分是什么?
【猜想假设】猜想①NaCl、Na2CO3 猜想②NaCl、Na2CO3、NaOH
猜想③NaCl、HCl、Na2CO3 猜想④:NaCl、HCl、猜想⑤:NaCl
上述猜想中,你认为不合理的是猜想③(填序号).
【实验探究】(1)甲同学取少量该溶液于试管中,向其中滴加无色酚酞溶液,发现溶液变红,据此,他认为猜想②是正确的,你认为他的结论是否合理?理由是什么?不合理,碳酸钠溶液也显碱性,能使无色的酚酞试液变红色.
(2)乙同学设计如下实验并得出正确结论,请你将下列实验报告补充完整.
【实验反思】下列物质①BaCl2溶液 ②Ca(OH)2溶液③Ca(NO3)2溶液 ④稀盐酸,能否代替乙同学实验中CaCl2溶液的是①③(填序号).
【提出问题】混合后溶液中溶质的成分是什么?
【猜想假设】猜想①NaCl、Na2CO3 猜想②NaCl、Na2CO3、NaOH
猜想③NaCl、HCl、Na2CO3 猜想④:NaCl、HCl、猜想⑤:NaCl
上述猜想中,你认为不合理的是猜想③(填序号).
【实验探究】(1)甲同学取少量该溶液于试管中,向其中滴加无色酚酞溶液,发现溶液变红,据此,他认为猜想②是正确的,你认为他的结论是否合理?理由是什么?不合理,碳酸钠溶液也显碱性,能使无色的酚酞试液变红色.
(2)乙同学设计如下实验并得出正确结论,请你将下列实验报告补充完整.
| 实验步骤 | 现象 | 结论 |
| ①取少量混合后的溶液于试管中,滴加足量CaCl2溶液 | 产生白色沉淀 | 猜想②成立 |
| ②过滤,再向滤液中滴加酚酞试液 | 变红色 |
3.关注健康,预防疾病.下列叙述正确的是( )
| A. | 氧、碳、氢、铁、氮、镁、钙都是人体中含有的常量元素 | |
| B. | 缺乏维生素A会引起坏血病 | |
| C. | 如果人体摄入的糖类过多,不仅容易发胖,还可能诱发疾病 | |
| D. | 老年人缺钙会患佝偻病 |
 如图为甲、乙、丙三种固体物质在水中的溶解度曲线,请回答:
如图为甲、乙、丙三种固体物质在水中的溶解度曲线,请回答:
