题目内容
 海洋是人类千万年来取之不尽、用之不竭的巨大资源宝库,开发前景广阔.
海洋是人类千万年来取之不尽、用之不竭的巨大资源宝库,开发前景广阔.
(1)目前海水淡化的方法有20多种,目前普遍采用______法
(2)“海水晒盐”后得到的卤水中含有MgCl2、KCl和MgSO4等物质,如图是它们的溶解度曲线示意图.
①设t1℃时MgCl2、KCl和MgSO4三种物质的溶解度分别为a、b、c,则它们的大小关系为______.
②将卤水加热到t2℃以上,根据溶解度曲线,首先析出的晶体是______(填名称).
(3)“海水制碱”过程中发生的分解反应是______(写方程式).
解:(1)海水淡化实际是将水中溶解的溶质除去,将水提炼出即可,目前海水淡化的方法有20多种,目前普遍采用多级闪急蒸馏的方法.
(2)①在t1℃时,氯化镁的曲线在最上面,溶解度最大,氯化钾和硫酸镁的溶解度曲线交于一点,它们的溶解度相等,
故a>b=c;
②将t1℃的MgCl2、KCl和MgSO4三种物质的饱和溶液加热到t2℃以上时,MgCl2、KCl的溶解度随温度的升高而增大,溶液变为不饱和溶液,而硫酸镁的溶解度随温度的升高而减小,所以有晶体析出.
(3)海水制碱过程是向饱和氨盐水中通入二氧化碳,析出碳酸氢钠晶体,然后将碳酸氢钠加热分解将得纯碱,化学反应方程式为NaCl+NH3+H2O+CO2=NaHCO3+NH4Cl;2NaHCO3 Na2CO3+H2O+CO2↑.碳酸氢钠分解是分解反应;
Na2CO3+H2O+CO2↑.碳酸氢钠分解是分解反应;
故答案为:(1)多级闪急蒸馏 (2)a>b=c 硫酸镁 (3)2NaHCO3 Na2CO3+H2O+CO2↑
Na2CO3+H2O+CO2↑
分析:(1)根据海水淡化的方法分析
(2)根据溶解度曲线的意义分析
(30根据海水制碱的过程发生的反应分析.
点评:本题以海水为载体,考查海水淡化的方法,溶解度曲线及海水制碱过程式中的反应,要了解海水资源的利用及制取过程是解答本题关键.
(2)①在t1℃时,氯化镁的曲线在最上面,溶解度最大,氯化钾和硫酸镁的溶解度曲线交于一点,它们的溶解度相等,
故a>b=c;
②将t1℃的MgCl2、KCl和MgSO4三种物质的饱和溶液加热到t2℃以上时,MgCl2、KCl的溶解度随温度的升高而增大,溶液变为不饱和溶液,而硫酸镁的溶解度随温度的升高而减小,所以有晶体析出.
(3)海水制碱过程是向饱和氨盐水中通入二氧化碳,析出碳酸氢钠晶体,然后将碳酸氢钠加热分解将得纯碱,化学反应方程式为NaCl+NH3+H2O+CO2=NaHCO3+NH4Cl;2NaHCO3
 Na2CO3+H2O+CO2↑.碳酸氢钠分解是分解反应;
Na2CO3+H2O+CO2↑.碳酸氢钠分解是分解反应;故答案为:(1)多级闪急蒸馏 (2)a>b=c 硫酸镁 (3)2NaHCO3
 Na2CO3+H2O+CO2↑
Na2CO3+H2O+CO2↑分析:(1)根据海水淡化的方法分析
(2)根据溶解度曲线的意义分析
(30根据海水制碱的过程发生的反应分析.
点评:本题以海水为载体,考查海水淡化的方法,溶解度曲线及海水制碱过程式中的反应,要了解海水资源的利用及制取过程是解答本题关键.

练习册系列答案
 全能练考卷系列答案
全能练考卷系列答案
相关题目
小刚设计实验探究铁、铜、银三种金属的活动性顺产并分析相关问题.请填空:
(1)他设计的四种实验方案,所需试剂如下:
①铜、银、硫酸亚铁溶液 ②铁、银、硫酸铜溶液
③银、硫酸亚铁溶液、硫酸铜溶液 ④铜、硫酸亚铁溶液,硝酸银溶液
上述方案中,正确的是______(填写序号).
(2)某化工厂生产过程中的残液含有硝酸银和硝酸铜两种物质.小刚取少量该残夜,分别盛在A、B两支试管中,再分别加入不同质量的铁粉,充分反应后过滤,分别取滤渣或滤液进行下表所示实验:
| 实验操作 | 实验现象 | 分析与结论 |
| 将A试管滤出的滤渣洗涤后加入到稀盐酸中 | 有气泡产生 | 从A试管得到的滤液中的溶质是______ |
| 向B试管得到的滤液中滴加少量稀盐酸 | 有白色沉淀生成 | B试管滤出的滤渣的成分是______ |
如图1是小华同学用氢氧化钠固体和水配制50g溶质质量分数25%的NaOH溶液的操作过程,该同学在称量氢氧化钠时,先在两个托盘上各放一张质量相同的纸,然后把药品直接放在纸上称量.
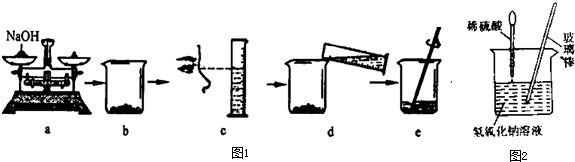
(1)a操作中的错误是______.
(2)下列操作中导致溶质质量分数偏低的是______(填字母).
A.a操作中砝码和氢氧化钠放错盘 B.b中烧杯用水洗涤后未干燥就使用
C.c操作中平视量筒凹液面最低处读数为37.5ml D.d操作中有少量水溅出
(3)小华同学用配制的溶液进行中和反应实验,(如图2所示装置),反应后为确定硫酸和氢氧化钠是否刚好完全反应,他取出一定量反应后的溶液于一支试管中,向其中滴入几滴无色酚酞试液,振荡,观察到酚酞试液不变色,于是他得出“两种物质已恰好完全中和”的结论.
①写出该中和反应的化学方程式______.
②小亮认为小华的结论不准确,他认为除了“两种物质已恰好完全中和”外还有第二种可能性,这种可能性是______.
③请你另外设计一个实验,探究上述烧杯中的溶液是否恰好完全中和.填写下表
| 实验 | 实验操作 | 实验现象 | 实验结论 |
| 甲 | 两种物质已恰好完全中和 | ||
| 乙 | 第二种可能性 |
(4)小华同学又用配制的溶液来做碱溶液与酚酞作用的实验.实验时,她发现了一个意外现象:在氢氧化钠溶液中滴入酚酞试液,溶液变成了红色,可是过了一会儿红色就消失了.这是什么原因呢?小华对这种意外现象的成因作了如下猜想:
A.可能是酚酞变质造成的;
B.可能是氢氧化钠溶液与空气中的二氧化碳反应的缘故;
C.可能与氢氧化钠溶液浓度大小有关.
依据所学的化学知识,你认为小华的猜想一定不成立的是______(填字母)






 化学小组的同学们准备制取一种气体.实验室现有稀硫酸、稀盐酸、块状石灰石,以及下列仪器:
化学小组的同学们准备制取一种气体.实验室现有稀硫酸、稀盐酸、块状石灰石,以及下列仪器: