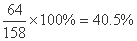题目内容
| ||
加热氯酸钾与二氧化锰制氧气的化学方程式为2KClO3
| ||
| △ |
由上述化学方程式不难看出:高锰酸钾中的氧元素只有部分转化为氧气单质,氯酸钾中的氧元素全部转化为氧气.故等质量的高锰酸钾和氯酸钾分别加热,充分反应后,高锰酸钾分解产生氧气的质量却远远小于氯酸钾分解产生氧气的质量.
故选:B.

解决问题常面临着方法的选择,面对不同的结果我们应继续探索。为得知15.8 g高锰酸钾完全分解能产生多少克氧气,小柯与小妍分别采取了以下方法:
| 小柯:实验测定法 | 小妍:计算法 |
| 小柯在老师的指导下,将15.8g高锰酸钾充分加热,得到氧气1300mL。 | 解:高锰酸钾中氧元素的质量分数
= 氧气的质量为:15.8g×40.5%=6.4g 答:15.8g高锰酸钾完全分解产生氧气6.4g。 |
请回答:
(1)在本实验条件下,氧气的密度为1.4×10-3g/mL,则由小柯的测量结果可算出
15.8 g高锰酸钾分解后所产生的氧气质量为——g(结果保留一位小数)。
(2)大家经过讨论,认为小妍的计算方法明显错误,本题不能采用该方法计算氧气质
量的一项理由是( )。
A.高锰酸钾中含氧元素
B.锰酸钾和二氧化锰中含氧元素
C.氧气中含氧元素
(3)请计算15.8 g高锰酸钾完全分解所产生的氧气质量为____________________g。
(4)若实验操作无误,不考虑实验中的误差,针对小柯的测定结果与你的计算结果,
请提出一种合理的猜测:_______________________________。
解决问题常面临着方法的选择,面对不同的结果我们应继续探索。为得知15.8 g高锰酸钾完全分解能产生多少克氧气,小柯与小妍分别采取了以下方法:
| 小柯:实验测定法 | 小妍:计算法 |
| 小柯在老师的指导下,将15.8g高锰酸钾充分加热,得到氧气1300mL。 | 解:高锰酸钾中氧元素的质量分数 =×100%21世纪教育网 = 氧气的质量为:15.8g×40.5%=6.4g
|
请回答:
(1)在本实验条件下,氧气的密度为1.4×10-3g/mL,则由小柯的测量结果可算出
15.8 g高锰酸钾分解后所产生的氧气质量为——g(结果保留一位小数)。
(2)大家经过讨论,认为小妍的计算方法明显错误,本题不能采用该方法计算氧气质
量的一项理由是( )。
A.高锰酸钾中含氧元素
B.锰酸钾和二氧化锰中含氧元素
C.氧气中含氧元素
(3)请计算15.8 g高锰酸钾完全分解所产生的氧气质量为____________________g。
(4)![]() 若实验操作无误,不考虑实验中的误差,针对小柯的测定结果与你的计算结果,
若实验操作无误,不考虑实验中的误差,针对小柯的测定结果与你的计算结果,
请提出一种合理的猜测:_______________________________。

 ×100%
×100%