题目内容
19.水是生命之源,请回答下列问题.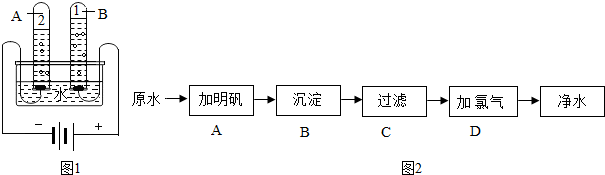
(1)如图1为电解水的装置.A试管中的气体是氢气,A试管中气体与B试管中气体的质量比为1:8,由实验得出,水是由氢元素和氧元素组成的.
(2)本市某水厂用原水(未经处理的水)生产自来水的净化步骤如图2表示:
①可以将大颗粒悬浮物杂质从水中除去的步骤是C(填标号).
②向水中加入活性炭(填写物质名称)吸附除去其中的异味.
③该厂生产的自来水是混合物(填“纯净物”或“混合物”).
(3)自然界的水因含有多种杂质而不能直接饮用.需要经过自来水厂处理后才能饮用.目前很多自来水厂用氯气进行消毒.消毒过程中常会发生如下化学反应,其反应的微观过程可用如图表示:
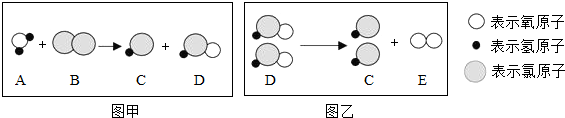
若D的化学式为HClO,写出图甲所示反应的化学方程式Cl2+H2O═HCl+HClO.
(4)小军将新制的氯气通入紫色石蕊试液中,惊奇地发现试液先变红,接着就褪色了.他查阅资料得知新制的氯水具有漂白性.为探究溶液褪色的原因,他设计了如下几个实验:
【实验准备】用紫色石蕊试液浸泡几朵小纸花,并晾干;加热少量新制的氯水,冷却后灌入喷壶.
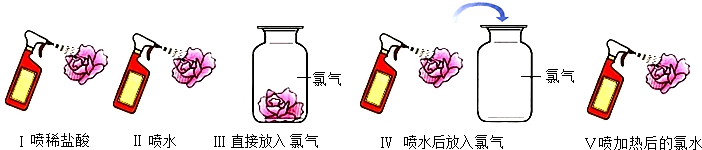 【实验现象】①实验Ⅰ:紫花变红; ②实验Ⅱ、Ⅲ:紫花不变色
【实验现象】①实验Ⅰ:紫花变红; ②实验Ⅱ、Ⅲ:紫花不变色③实验Ⅳ:紫花先变红后褪色 ④实验Ⅴ:紫花变红,不褪色
【实验结论】新制氯水中具有漂白性的物质是HClO(写化学式).
分析 (1)电解水时,正极产生的是氧气,负极产生的是氢气,氧气和氢气的体积比约为1:2;
(2)过滤可以把不溶于水的物质除去;
活性炭具有吸附性,能够吸附水中的色素和异味;
(3)根据反应的微观粒子示意图可以书写反应的化学方程式;
(4)根据实验现象可以判断相关方面的问题.
解答 解:(1)如图1为电解水的装置.A试管中的气体是氢气,A试管中气体与B试管中气体的质量比为1:8,由实验得出,水是由氢元素和氧元素组成的.
故填:氢气;1:8;氢元素和氧元素.
(2)①可以将大颗粒悬浮物杂质从水中除去的步骤是C,通过过滤可以除去大颗粒悬浮物杂质;
②向水中加入活性炭可以吸附除去其中的异味;
③该厂生产的自来水中仍然含有一些溶于水的物质,是混合物.
故填:C;活性炭;混合物.
(3)若D的化学式为HClO,则氯气和水反应生成了盐酸和次氯酸,反应的化学方程式为:Cl2+H2O═HCl+HClO.
故填:Cl2+H2O═HCl+HClO.
(4)【实验现象】
实验Ⅰ:因为稀盐酸显酸性,能使石蕊试液变红色,因此紫花变红.
故填:紫花变红.
【实验结论】
由实验Ⅴ可知,喷加热后的氯水时,紫花变红,不褪色,说明次氯酸受热分解生成了稀盐酸和氧气后,不能使紫花褪色,进一步说明新制氯水中具有漂白性的物质是HClO.
故填:HClO.
点评 合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.

练习册系列答案
 宝贝计划期末冲刺夺100分系列答案
宝贝计划期末冲刺夺100分系列答案 能考试全能100分系列答案
能考试全能100分系列答案
相关题目
11.下列叙述中,正确的是( )
| A. | 均一、稳定的液体一定是溶液 | |
| B. | 能电离出H+的化合物一定是酸 | |
| C. | 物质跟氧气发生的反应,一定是氧化反应 | |
| D. | 置换反应一定要在溶液中进行 |