题目内容
某兴趣小组对氧化铜与过量碳粉充分反应后的混合物重新进行实验,以测定混合物中铜的质量分数(实验装置如下图所示,铁架台等固定装置已略去,装置气密性良好)。

(查阅资料)①浓硫酸不与CO2反应,具有吸水性,常用作干燥剂。
②碱石灰主要成分为CaO和NaOH,可吸收H2O和CO2。
(供选药品)
铜粉(含碳)样品、二氧化锰、碱石灰;浓硫酸、5%过氧化氢溶液、澄清石灰水、氢氧化钠溶液。
部分实验步骤如下:
I.在硬质玻璃管中加入质量为m的铜粉(含碳)样品,丁中装入药品后的质量为m1。
Ⅱ.控制甲中的装置,缓缓产生气体。
Ⅲ.点燃酒精灯,当玻璃管中的药品充分反应后,熄灭酒精灯。
Ⅳ.继续通入气体,直到玻璃管冷却,称量丁的质量为m2。
试回答下列问题:
(1)甲处方框内应选用下列装置中的_____,该装置中发生反应的化学方程式为_____。

(2)装置戊的作用为_____。
(3)样品中铜的质量的表达式为_____。
(4)若无装置乙,会导致测得铜的质量分数_____(填“偏小’’‘‘偏大"或“无影响")。
 全能测控一本好卷系列答案
全能测控一本好卷系列答案除去下列物质中的少量杂质,所选用试剂或方法正确的是( )
选项 | 物质 | 所含杂质 | 试剂及方法 |
A | Fe | Cu | 足量的稀盐酸,过滤 |
B | CuSO4溶液 | H2SO4 | 加入适量的铜粉 |
C | CaO | CaCO3 | 加入足量的水溶解,过滤 |
D | FeCl2溶液 | CuCl2溶液 | 加入过量的铁粉,过滤 |
A.A B.B C.C D.D
某同学利用如图所示装置,选用不同可燃物测定空气里氧气的含量。实验起始时在集气瓶中装入少量水,并将水面上方空间分为五等份。将燃烧匙内的可燃物加热至燃烧或红热后,伸入瓶中塞紧瓶塞。冷却至室温后打开弹簧夹,记录数据如下表(装置的气密性良好)。

实验编号 | 可燃物 | 进入集气瓶中水的高度 |
① | 镁带 | 等于3格 |
② | 铁丝 | 几乎为0 |
③ | 红磷 | 约为0.6格 |
④ | 红磷 | 约为1.5格 |
下列有关解释不合理的是
A.实验①可能原因是:镁带除与氧气反应外,还能与空气中的其他气体反应
B.实验②可能原因是:铁丝燃烧消耗的氧气与生成的气体体积相等
C.实验③可能原因是:红磷量太少,集气瓶中的氧气未完全反应
D.实验④可能原因是:红磷点燃后,插入燃烧匙时,未迅速塞紧瓶塞,有部分空气逸出
“黄铜”是铜和锌的合金,为了测定某黄铜样品中锌的质量分数,甲、乙、丙三位同学分别进行实验,实验数据如下。(烧杯质量均为56.5克)
1 | 甲 | 乙 | 丙 |
烧杯+稀盐酸质量 | 98.0g | 93.0g | 93.0g |
加入黄铜样品质量 | 10.0g | 12.0g | 10.0g |
充分反应后,烧杯+剩余物质质量 | 107.9g | 104.9g | 102.9g |
请回答下列问题:
(1)_____同学用的稀盐酸和黄铜样品恰好完全反应,他制取的氢气的质量是_____。
(2)计算黄铜样品中锌的质量分数_____(要求写出计算过程)。
(3)计算盐酸的质量分数为_____。


 B.
B. C.
C. D.
D.
 ”、“
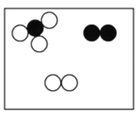
”、“ ”分别表示不同元素的原子,则其中表示化合物的是
”分别表示不同元素的原子,则其中表示化合物的是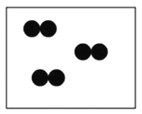 B.
B.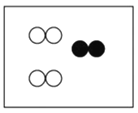 C.
C. D.
D.