题目内容
15. 聪聪同学将稀硫酸加入到一定质量的金属锌中反应,测出放出气体的质量与加入稀硫酸的质量关系如图所示.试求:
聪聪同学将稀硫酸加入到一定质量的金属锌中反应,测出放出气体的质量与加入稀硫酸的质量关系如图所示.试求:(1)所用稀硫酸的溶质的质量分数.
(2)若用98%的浓硫酸配制上述反应所需的稀硫酸,需98%浓硫酸的质量.
分析 (1)根据图中数据可以判断生成氢气的质量;根据氢气的质量可以计算稀硫酸中硫酸的质量,进一步可以计算所用硫酸溶液中溶质的质量分数;
(2)根据溶质质量不变原理,求出需要98%的浓硫酸的质量.
解答 解:
(1)由图中可知,完全反应后生成H2的质量为0.2g.
设所用硫酸溶液中溶质的质量为x,
Zn+H2SO4═ZnSO4+H2↑,
98 2
x 0.2g
$\frac{98}{x}=\frac{2}{0.2g}$
x=9.8g
所用稀硫酸的溶质的质量分数=$\frac{9.8g}{98g}×$100%=10%
(2)设需要98%的浓硫酸的质量为y
y×98%=98g×10% 解得:y=10g
答案:
(1)所用稀硫酸的溶质的质量分数为10%
(2)需98%浓硫酸的质量为10g
点评 此题是根据化学方程式及溶质质量分数的计算题,该题比较简单,属于最基本类型的计算题.计算时注意计算数据的准确性.

练习册系列答案
相关题目
6.生活中的下列过程,一定发生了化学变化的是( )
| A. | 酿葡萄酒 | B. | 编中国结 | C. | 折千纸鹤 | D. | 绘水墨画 |
20.向CuSO4溶液中加入一定质量的铝粉,完全反应后过滤,得滤渣和蓝色滤液.下列说法正确的是( )
| A. | 滤液中只有CuSO4 | B. | 向滤渣中滴加稀盐酸,无气泡产生 | ||
| C. | 滤液中只有Al2(SO4)3 | D. | 滤渣中一定有Cu,可能有Al |
7.金属钛(Ti)抗腐蚀性能好,露置于空气中数年,仍光亮如初.以金红石(主要成分是TiO2)为原料生产金属钛的步骤主要有:①在高温下,向金红石与焦炭的混合物中通入氯气(Cl2),得到TiCl4和一种可燃性气体;②在稀有气体环境和加热条件下,用Mg和TiCl4反应得到Ti和MgCl2.下列说法不正确的是( )
| A. | 金属钛在常温下不与O2反应 | |
| B. | ②中的稀有气体的作用是隔绝空气 | |
| C. | ①中的反应TiO2+C+2Cl2$\frac{\underline{\;高温\;}}{\;}$TiCl4+CO2 | |
| D. | ②中发生的反应为置换反应 |
4.下列图示实验操作中,正确的是( )
| A. | 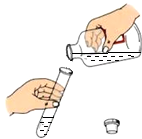 倾倒液体 | B. |  闻气味 | C. | 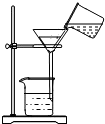 过滤 | D. | 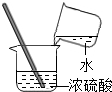 稀释浓硫酸 |
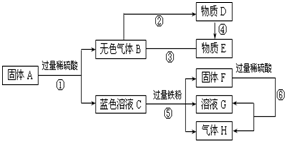
 已知A、B、C、D、E是初中化学常见的不同类别的物质,C的水溶液呈蓝色,D是一种红色固体,B→D的反应过程较为复杂,D→B的反应用于冶金工业,图中“-”表示相连物质可以发生反应,“→”表示一种物质生成另一种物质(部分反应物、生成物及反应条件省略).
已知A、B、C、D、E是初中化学常见的不同类别的物质,C的水溶液呈蓝色,D是一种红色固体,B→D的反应过程较为复杂,D→B的反应用于冶金工业,图中“-”表示相连物质可以发生反应,“→”表示一种物质生成另一种物质(部分反应物、生成物及反应条件省略).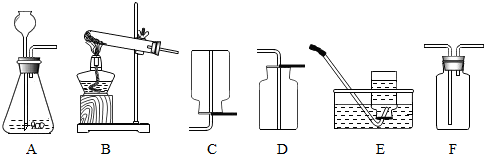
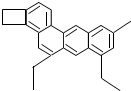 化学家TimRichard将分子结构简式像小狗的某有机物(如图所示),取名为“小狗烯”(化学式为C26H26),请计算:
化学家TimRichard将分子结构简式像小狗的某有机物(如图所示),取名为“小狗烯”(化学式为C26H26),请计算: