题目内容
16.科学家研发出一种铝镓(Ga)合金,从物质分类的角度看,铝镓合金属于混合物(填“纯净物”或“混合物”);用该合金与铝片相互刻画,发现铝片上有划痕,说明合金的硬度大于组成它的纯金属的硬度.分析 根据合金的组成以及合金的特点来分析.
解答 解:铝镓合金属于多种物质组成的混合物;合金要比它的成分金属的硬度变大熔点变低,所以两块金属片相互刻划后,在铝片上有明显的划痕,说明硬度比合金小;
故填:混合物;合金的硬度大.
点评 本题难度不大,可依据合金的性能分析解答.

练习册系列答案
相关题目
6.下列物质属于有机物的是( )
| A. | 硫酸 | B. | 二氧化碳 | C. | 碳酸钙 | D. | 甲烷 |
7.如表是甲、乙、丙三种物质的部分溶解度(单位:g/100g水),请回答.
①10℃时,甲物质的溶解度是35.8g/100g水;
②三种物质中溶解度受温度影响较大的是乙;
③物质在水中的溶解性与其溶解度(20℃)的关系示意图如图1,则丙物质在水中的溶解性是微溶于水;

④30℃时,乙物质饱和溶液的溶质质量分数是$\frac{45.8g}{100g+45.8g}×100%$;(列式即可,不要求计算)
⑤50℃时,三种物质的溶解度由大到小的顺序是乙、甲、丙;
⑥向不同温度的100g水中分别放入等质量的乙物质,保持温度不变,溶解情况如图2所示.相关分析正确的是bd;
a.溶液温度:Ⅰ>Ⅱ>Ⅲ>Ⅳ
b.溶液质量:Ⅰ=Ⅱ>Ⅲ>Ⅳ
c.溶液Ⅰ一定是不饱和溶液
d.使Ⅳ中的固体全部溶解,溶质质量分数可能不变.
| 温度(℃) | 10 | 20 | 30 | 40 | 50 | 60 |
| 甲 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 |
| 乙 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110.0 |
| 丙 | 0.182 | 0.165 | 0.160 | 0.141 | x | 0.121 |
②三种物质中溶解度受温度影响较大的是乙;
③物质在水中的溶解性与其溶解度(20℃)的关系示意图如图1,则丙物质在水中的溶解性是微溶于水;

④30℃时,乙物质饱和溶液的溶质质量分数是$\frac{45.8g}{100g+45.8g}×100%$;(列式即可,不要求计算)
⑤50℃时,三种物质的溶解度由大到小的顺序是乙、甲、丙;
⑥向不同温度的100g水中分别放入等质量的乙物质,保持温度不变,溶解情况如图2所示.相关分析正确的是bd;
a.溶液温度:Ⅰ>Ⅱ>Ⅲ>Ⅳ
b.溶液质量:Ⅰ=Ⅱ>Ⅲ>Ⅳ
c.溶液Ⅰ一定是不饱和溶液
d.使Ⅳ中的固体全部溶解,溶质质量分数可能不变.
11.如图所示的实验操作不正确的是( )
| A. |  取用液体 | B. |  称量NaCl质量 称量NaCl质量 | C. |  闻气体的气味 | D. |  读取液体体积 |
1.将燃着的镁带伸入盛有二氧化碳集气瓶中,镁带继续剧烈燃烧,反应的化学方程式为:
2Mg+CO2$\frac{\underline{\;点燃\;}}{\;}$2MgO+C,下列叙述错误的是( )
2Mg+CO2$\frac{\underline{\;点燃\;}}{\;}$2MgO+C,下列叙述错误的是( )
| A. | 该反应中镁发生了氧化反应 | |
| B. | 该反应中元素的化合价都发生了改变 | |
| C. | 该反应说明了燃烧不一定都需要有氧气 | |
| D. | 镁着火时不能用二氧化碳灭火 |
8.下列物质属于氧化物的是( )
| A. | 冰水混合物 | B. | 碳水化合物 | C. | 澄清石灰水 | D. | 消毒水 |
5.为探究气体X的组成,某兴趣小组进行如图所示实验(固定装置未画出).
【实验装置】
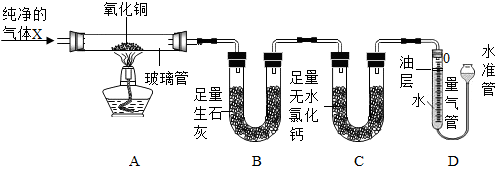
【查阅资料】
(1)加热条件下,气体X能与氧化铜反应生成铜、水和氮气.
(2)生石灰与气体X不反应,无水氯化钙可吸收气体X.
(3)本实验条件下,装置内空气中的水、二氧化碳的影响可忽略不计.
【实验步骤】
(1)连接仪器,并检查装置气密性.
(2)准确称取2.40g氧化铜,装入A装置的玻璃管中,并在B、C、D中装入相应物质.
(3)测量并记录反应前的相关数据Ⅰ(见表).
(4)连接A、B、C装置,将气体X缓缓通入一段时间后,连接上D装置,再开始加热.(利用装置D中液面在反应前、后的刻度差,可测得生成的氮气的体积)
(5)当A装置中氧化铜反应完全后,停止加热,并继续通入气体X至玻璃管冷却.,再次测量并记录反应后的相关数据Ⅱ.
【相关数据】
注:如表中氮气的质量是通过D装置收集的氮气体积,并通过氮气的密度计算得到.
【回答问题】
(1)B装置中氧化钙吸水的原理为CaO+H2O=Ca(OH)2(用化学方程式表示).
(2)实验中,A装置的玻璃管中可观察到的现象是粉末由黑色逐渐变红.当观察到量气管内液面不再下降,说明氧化铜已完全反应.停止加热,继续通入气体X至玻璃管冷却的目的是防止灼热的铜被氧化.
(3)分析实验测量的数据,生成水的质量为0.54g,氧化铜中氧元素的质量为0.48g.
由此推知,气体X中没有(填“有”或“没有”或“可能有”)氧元素.
(4)气体X的化学式为NH3.
【实验装置】

【查阅资料】
(1)加热条件下,气体X能与氧化铜反应生成铜、水和氮气.
(2)生石灰与气体X不反应,无水氯化钙可吸收气体X.
(3)本实验条件下,装置内空气中的水、二氧化碳的影响可忽略不计.
【实验步骤】
(1)连接仪器,并检查装置气密性.
(2)准确称取2.40g氧化铜,装入A装置的玻璃管中,并在B、C、D中装入相应物质.
(3)测量并记录反应前的相关数据Ⅰ(见表).
(4)连接A、B、C装置,将气体X缓缓通入一段时间后,连接上D装置,再开始加热.(利用装置D中液面在反应前、后的刻度差,可测得生成的氮气的体积)
(5)当A装置中氧化铜反应完全后,停止加热,并继续通入气体X至玻璃管冷却.,再次测量并记录反应后的相关数据Ⅱ.
| 数据编号 测量项目 | Ⅰ | Ⅱ |
| 玻璃管(含药品)的质量/g | 54.40 | 53.92 |
| B装置(含药品)的质量/g | 104.00 | 104.54 |
| 氮气的质量/g | / | 0.28 |
注:如表中氮气的质量是通过D装置收集的氮气体积,并通过氮气的密度计算得到.
【回答问题】
(1)B装置中氧化钙吸水的原理为CaO+H2O=Ca(OH)2(用化学方程式表示).
(2)实验中,A装置的玻璃管中可观察到的现象是粉末由黑色逐渐变红.当观察到量气管内液面不再下降,说明氧化铜已完全反应.停止加热,继续通入气体X至玻璃管冷却的目的是防止灼热的铜被氧化.
(3)分析实验测量的数据,生成水的质量为0.54g,氧化铜中氧元素的质量为0.48g.
由此推知,气体X中没有(填“有”或“没有”或“可能有”)氧元素.
(4)气体X的化学式为NH3.
