题目内容
6.如图是某化学学习小组设计的用一氧化碳还原氧化铁的实验装置.请回答以下问题:
(1)该装置存在的一个主要问题是缺少尾气处理装置;你的改进方法是在装置最后的导管口放置一点燃的酒精灯.
(2)实验过程中,图中A处能观察到的实验现象是红棕色粉末慢慢变成黑色,发生反应的化学方程式为Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;
(3)B处观察到的实验现象是澄清的石灰水变浑浊,发生反应的化学方程式为CO2+Ca(OH)2=CaCO3↓+H2O.
分析 (1)根据尾气中含有有毒的一氧化碳来分析;
(2)根据化学反应的原理以及化学方程式的写法来分析;
(3)根据二氧化碳的性质与化学方程式的写法来分析.
解答 解:(1)反应结束后的尾气中含有有毒的一氧化碳气体,为了防止造成空气的污染,需要将尾气点燃处理;故填:缺少尾气处理装置;在装置最后的导管口放置一点燃的酒精灯;
(2)在高温的条件下,一氧化碳将氧化铁还原为铁,同时生成二氧化碳,所以装置A中的现象是红棕色粉末慢慢变成黑色;故填:红棕色粉末慢慢变成黑色;Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;
(3)二氧化碳与氢氧化钙反应生成碳酸钙沉淀和水,所以观察到B处的现象是澄清的石灰水变浑浊;故填:澄清的石灰水变浑浊;CO2+Ca(OH)2=CaCO3↓+H2O.
点评 本题主要考查了一氧化碳的性质、一氧化碳还原氧化铁的实验.特别要掌握一氧化碳还原氧化铁的实验原理和实验中的一些注意事项,难度较大.

练习册系列答案
相关题目
14.某混合物中含有Fe2O3、Fe3O4、FeO三种物质,已知该混合物中铁元素与氧元素的质量比为21:8,则该混合物中Fe2O3、Fe3O4、FeO的质量比可能为( )
| A. | 1:1:1 | B. | 160:232:144 | C. | 320:232:144 | D. | 320:232:72 |
1.实验室现有足量的20%的NaOH的溶液和蒸馏水,欲配制10%的NaOH溶液100g,需要20%的NaOH溶液( )
| A. | 95 g | B. | 50 g | C. | 100 g | D. | 10 g |
11.对于下列化学用语,有关说法正确的是( )
①O2②Mg2+③SO2④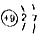 ⑤
⑤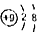
①O2②Mg2+③SO2④
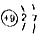 ⑤
⑤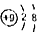
| A. | ①可表示两个氧原子 | B. | ③中硫元素的化合价为+4 | ||
| C. | ②和⑤均表示阳离子 | D. | ④和⑤表示的微粒化学性质相同 |
18.下列物质中含有氧气分子的是( )
| A. | 过氧化氢 | B. | 二氧化锰 | C. | 液态空气 | D. | 二氧化碳 |
15.下列除去杂质的方法,正确的是( )
| A. | CO(CO2)通过灼热的氧化铜 | |
| B. | 氯化钙溶液(盐酸)加过量的碳酸钙后过滤 | |
| C. | NaOH溶液(Na2CO3)加适量稀盐酸 | |
| D. | 铁粉(氧化铜粉末)加入足量稀硫酸后过滤 |