题目内容
【题目】城市自来水的处理过程如图所示:
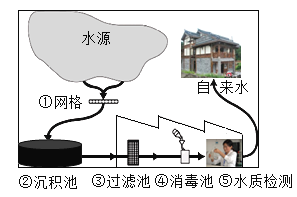
(1)步骤①网格净水原理类似于步骤______(选填图中②~⑤的序号)。
(2)步骤②所起的作用是______(填序号)。
A 杀死水中的细菌
B 减少水中氧气
C 使泥沙沉积至底部
D 分解有毒物质
(3)生活中将自来水软化的常用方法是______。区分软水和硬水的试剂是____。
【答案】③ C 煮沸 肥皂水
【解析】
(1)步骤①网格净水可以将大颗粒不溶物与水分离,原理类似于过滤,相当于步骤③。
(2)步骤②沉积池所起的作用是:
A、消毒池的用作是杀死水中的细菌;故选项错误;
B、沉淀池不能减少水中氧气;故选项错误;
C、沉积池的作用是使泥沙沉积至底部,经过滤后出去;故选项正确;
D、消毒池可以处理有毒物质,使水达到饮用标准;故选项错误;
故选:C。
(3)生活中将自来水软化的常用方法是加热、煮沸,因为:煮沸过程中可以使钙离子、镁离子形成沉淀,使其硬度降低。区分软水和硬水的试剂是:肥皂水;将其分别混合搅拌后,浮渣多,泡沫少的是硬水;反之是软水。

练习册系列答案
相关题目