题目内容
某化学兴趣小组的同学在实验室配制溶质质量分数为7.3%的稀盐酸,并用其测定某氢氧化钠溶液溶质的质量分数.右图表示用上述配制的稀盐酸与20g某氢氧化钠溶液发生反应过程中,使用数字传感仪测得溶液温度变化的曲线.(1)20℃以后温度变化的原因是______,______.
(2)当加入25g盐酸溶液时,所得溶液中的微粒有:______(用化学符号表示).
(3)试列式计算:某氢氧化钠溶液的溶质质量分数.
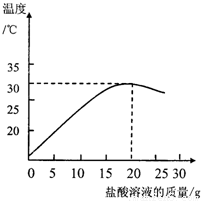
【答案】分析:(1)根据中和反应反应完毕后不再放出热量来考虑;(2)加入25g盐酸溶液时盐酸过量,通过分析反应后存在的溶质考虑溶液中的离子;(3)根据图象可知反应完毕消耗盐酸的质量为20g,再乘以盐酸的质量分数,算出氯化氢的质量,再通过计算算出氢氧化钠的质量,再除以氢氧化钠溶液的质量即可.
解答:解:(1)中和反应反应完毕后不再放出热量,这时由于热量散失温度会降低,加入的过量盐酸吸热也会降低温度;
(2)由于盐酸与氢氧化钠反应生成氯化钠和水,加入25g盐酸溶液时盐酸过量,所以反应后的溶液中含有氯化钠、盐酸,氯化钠电离出钠离子和氯离子,盐酸中电离出氢离子和氯离子,溶液中还存在水分子;
(3)通过图表可知消耗盐酸的质量为20g,因为盐酸的质量分数为7.3%,所以消耗氯化氢质量为20g×7.3%=1.46g,设与1.46g氯化氢反应需要氢氧化钠的质量为X则:
NaOH+HCl=NaCl+H2O
40 36.5
X 1.46g
根据: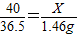 解得X=1.6g,所以氢氧化钠溶液的溶质质量分数为:
解得X=1.6g,所以氢氧化钠溶液的溶质质量分数为: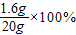 =8%.
=8%.
故答案为:(1)热量散失;后来加入的过量盐酸吸热;(2)Na+、H+、Cl-、H2O;(3)8%.
点评:解答本题的关键是要知道中和反应放出热量,反应完毕就会停止放热,热量开始散失而降低,过量的盐酸也会吸热;反应后溶液中的离子要考虑反应后溶液中的溶质;解答本题还需要结合图表中数据分析出参加反应的氯化氢的质量.
解答:解:(1)中和反应反应完毕后不再放出热量,这时由于热量散失温度会降低,加入的过量盐酸吸热也会降低温度;
(2)由于盐酸与氢氧化钠反应生成氯化钠和水,加入25g盐酸溶液时盐酸过量,所以反应后的溶液中含有氯化钠、盐酸,氯化钠电离出钠离子和氯离子,盐酸中电离出氢离子和氯离子,溶液中还存在水分子;
(3)通过图表可知消耗盐酸的质量为20g,因为盐酸的质量分数为7.3%,所以消耗氯化氢质量为20g×7.3%=1.46g,设与1.46g氯化氢反应需要氢氧化钠的质量为X则:
NaOH+HCl=NaCl+H2O
40 36.5
X 1.46g
根据:
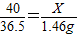 解得X=1.6g,所以氢氧化钠溶液的溶质质量分数为:
解得X=1.6g,所以氢氧化钠溶液的溶质质量分数为: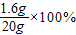 =8%.
=8%.故答案为:(1)热量散失;后来加入的过量盐酸吸热;(2)Na+、H+、Cl-、H2O;(3)8%.
点评:解答本题的关键是要知道中和反应放出热量,反应完毕就会停止放热,热量开始散失而降低,过量的盐酸也会吸热;反应后溶液中的离子要考虑反应后溶液中的溶质;解答本题还需要结合图表中数据分析出参加反应的氯化氢的质量.

练习册系列答案
相关题目
 12、碳酸氢钠(NaHCO3)俗称小苏打,常用于食品和医药工业.某化学兴趣小组的同学对碳酸氢钠的性质进行探究.
12、碳酸氢钠(NaHCO3)俗称小苏打,常用于食品和医药工业.某化学兴趣小组的同学对碳酸氢钠的性质进行探究.


 (2012?烟台)某化学兴趣小组的同学用如图所示装置进行实验(装置气密性良好),先关闭止水夹,将足量的氢氧化钠溶液滴入烧瓶中,充分吸收掉二氧化碳后,再打开止水夹.
(2012?烟台)某化学兴趣小组的同学用如图所示装置进行实验(装置气密性良好),先关闭止水夹,将足量的氢氧化钠溶液滴入烧瓶中,充分吸收掉二氧化碳后,再打开止水夹. 某化学兴趣小组的同学在实验室配制质量分数为8%的氢氧化钠溶液,并用其测定某稀盐酸中溶质的质量分数.
某化学兴趣小组的同学在实验室配制质量分数为8%的氢氧化钠溶液,并用其测定某稀盐酸中溶质的质量分数.