题目内容
2.为测定实验室一瓶放置已久的烧碱中NaOH含量,取5O.Og烧碱样品,溶于一定量的水得到200g溶液,再加入200g稀硫酸(足量)充分搅拌到不再放出气泡为止,称量溶液为395.6g.请计算:(1)反应产生的CO2的质量为4.4g.
(2)样品中NaOH的质量分数是多少?(写出计算过程)
分析 (1)根据质量守恒定律,反应过程中所生成的气体的质量等于反应前后溶液质量的减少;
(2)样品中NaOH的质量分数等于样品中NaOH的质量除以样品的总质量,所以我们可以根据上一步所求得氧气的质量,根据质量守恒定律,求得样品中NaOH的质量,而后再求样品中NaOH的质量分数.
解答 解:(1)根据质量守恒定律,反应前后溶液质量的减少就等于反应过程中所生成的气体的质量,所以反应产生的CO2的质量为200g+200g-395.6g=4.4g.
故答案为:4.4
(2)解:设所取样品中含有Na2CO3的质量为x.
Na2CO3+H2SO4═Na2SO4+H2O+CO2↑
106 44
x 4.4g
$\frac{106}{x}=\frac{44}{4.4g}$
解之得:x=10.6g
样品中NaOH的质量分数是:$\frac{50g-10.6g}{50g}×$100%═78.8%
答案:
(1)4.4
(2)烧碱样品中NaOH的百分含量为78.8%.
点评 此题主要是在碱的化学性质的基础上考查有关质量守恒定律的有关知识,以及混合物中质量分数的计算问题,注重学生综合能力的培养,是中考的考点之一.

练习册系列答案
 暑假作业海燕出版社系列答案
暑假作业海燕出版社系列答案 本土教辅赢在暑假高效假期总复习云南科技出版社系列答案
本土教辅赢在暑假高效假期总复习云南科技出版社系列答案 暑假作业北京艺术与科学电子出版社系列答案
暑假作业北京艺术与科学电子出版社系列答案
相关题目
12.摩尔(符号:mol)是物质的量的单位.1mol任何物质的质量以克为单位时,在数值上都与其相对分子质量相等,如:1mol H2O的质量为18克;标准状况下,1mol任何气体的体积为22.4升.则标准状况下,33.6升甲烷的质量是( )克.
| A. | 16 | B. | 24 | C. | 32 | D. | 40 |
7.图实验不能说明的是( )


| A. | 浓盐酸具有挥发性 | |
| B. | 分子不停地运动 | |
| C. | 构成物质的微粒不同,性质不同 | |
| D. | 化学反应的实质是分子破裂为原子,原子重新结合成新分子 |
14.20℃时,取甲、乙、丙、丁四种纯净物各20g,分别加入到四个各盛有50g水的烧杯中,充分溶解,其溶解情况如下表:
下列说法正确的是( )
| 物质 | 甲 | 乙 | 丙 | 丁 |
| 未溶解固体的质量/g | 4.2 | 2 | 0 | 9.2 |
| A. | 所得溶液一定都是饱和溶液 | |
| B. | 20℃时四种物质溶解度的关系为:丁>甲>乙>丙 | |
| C. | 丁溶液中溶质质量分数一定最大 | |
| D. | 所得溶液的质量关系为:丙>乙>甲>丁 |
11.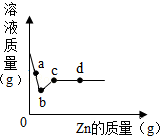 向一定质量Mg (NO3)2、AgNO3和Cu(NO3)2的混合溶液中加入Zn,溶液质量与加入Zn的质量关系如图所示,下列说法正确的是( )
向一定质量Mg (NO3)2、AgNO3和Cu(NO3)2的混合溶液中加入Zn,溶液质量与加入Zn的质量关系如图所示,下列说法正确的是( )
 向一定质量Mg (NO3)2、AgNO3和Cu(NO3)2的混合溶液中加入Zn,溶液质量与加入Zn的质量关系如图所示,下列说法正确的是( )
向一定质量Mg (NO3)2、AgNO3和Cu(NO3)2的混合溶液中加入Zn,溶液质量与加入Zn的质量关系如图所示,下列说法正确的是( )| A. | a点溶液中的溶质有3种 | |
| B. | c点溶液中溶质为Mg (NO3)2、Zn(NO3)2 | |
| C. | 若取b~c段溶液,滴加稀盐酸,有白色沉淀 | |
| D. | 取d点的固体,加入稀盐酸,有气泡产生 |
12.下面是4位同学对“化学与健康”这一话题发表的见解,其中正确的是( )
| A. |  小丽 | B. |  小明 | ||
| C. |  小刚 | D. |  小强 |

 A、B、C、D、E是初中化学常见的五种不同类别的物质,其中A、B、C中含有相同 元素,B是导致“温室效应”的一种气体.图中“-”示相连的物质在一定条件下可以发生反应,“→”表示物质间存在转化关系.
A、B、C、D、E是初中化学常见的五种不同类别的物质,其中A、B、C中含有相同 元素,B是导致“温室效应”的一种气体.图中“-”示相连的物质在一定条件下可以发生反应,“→”表示物质间存在转化关系.