题目内容
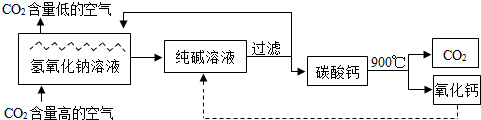
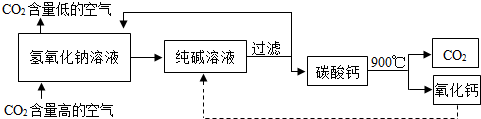
二氧化碳的“捕捉”与“封存”是实现温室气体减排的重要途径之一。实际生产中,经常利用足量NaOH溶液来“捕捉”CO2,流程图如下(部分条件及物质未标出)。

(1)分离室中进行的操作是 。
(2)该流程图所标出的物质中,溶于水放出大量热的氧化物是 ,与水发生反应的化学方程式为 。
(3)“捕捉室”中发生的化学反应为2NaOH CO2
→ Na2CO3
CO2
→ Na2CO3 M,则M的化学式为 ;整个“捕捉”过程中,可循环使用的物质是 。
M,则M的化学式为 ;整个“捕捉”过程中,可循环使用的物质是 。
【答案】
(1)过滤
(2)氧化钙(或CaO) CaO+H2O =Ca(OH)2
(3)H2O CaO、NaOH (或氧化钙、氢氧化钠 错漏一个不得分)
【解析】
试题分析:(1)通过分离室把固体和液体分离开了,故该操作是过滤;(2)氧化钙与水反应会释放出大量的热,氧化钙与水反应生成氢氧化钙,根据这些信息书写化学方程式;(3)由于反应物的分中含有2个钠原子、4个氧原子、2个氢原子和1个碳原子,而已知的生成物质的分子中含有2个钠原子、1个碳原子和3个氧原子,根据质量守恒定律可知,M中一定含有1个氧原子和2个氢原子,故其化学式为H2O;从图示信息可以看出CaO和NaOH可以循环使用。
考点:过滤,氧化钙的性质,质量守恒定律。

练习册系列答案
 状元坊全程突破导练测系列答案
状元坊全程突破导练测系列答案
相关题目
二氧化碳的捕捉与封存是实现温室气体减排的重要途径之一,科学家利用NaOH溶液喷淋“捕捉”空气中的CO2(如下图).则关于该方法的叙述正确的是( )
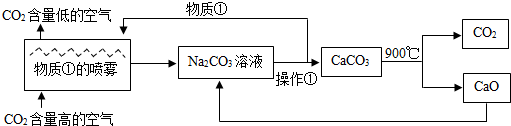

| A、该方法中包含复分解反应、分解反应、置换反应等 | B、物质①是Ca(OH)2溶液 | C、操作①是过滤 | D、整个过程至少有NaOH和CO2两种物质可以循环利用 |