题目内容
13.某气体由CO、CO2和N2组成,测得其中含氧元素的质量分数为60%,则该气体中含N2的质量分数可能是( )| A. | 20% | B. | 25% | C. | 40% | D. | 50% |
分析 根据一氧化碳中氧元素的质量分数,二氧化碳中氧元素的质量分数,氮气中不含氧元素,氧元素质量分数是零,假设两个极端值,只含有一氧化碳和氮气,或只含有二氧化碳和氮气,然后求出氮气的质量分数进行解答.
解答 解:一氧化碳中氧元素的质量分数为:$\frac{16}{28}$×100%=57%,
二氧化碳中氧元素的质量分数为:$\frac{32}{44}$×100%=73%,
氮气中不含氧元素,所以氧元素质量分数为0%,
假设只含有氮气和一氧化碳,所以氮气的质量分数小于43%,
假设只含有氮气和二氧化碳,设混合气氮气质量为x,二氧化碳质量为y,混合气总质量为a,
$\left\{\begin{array}{l}{x+y=a}\\{x×0%+y×73%=60%×a}\end{array}\right.$
解答:$\left\{\begin{array}{l}{x=0.18a}\\{y=0.82a}\end{array}\right.$
所以氮气的质量分数为:$\frac{0.18a}{a}$×100%=18%,
由于该混合气由氮气、二氧化碳、一氧化碳混合而成,所以混合气体中含N2的质量分数大于18%,
综合分析可知,氮气的质量分数在18%和43%之间,故选:ABC.
点评 本题是一道考查混合物质中根据某元素的质量分数来求的另外几种物质或者元素的质量分数,方法有多种,但多用极值法做类似的题目;难度较大,培养学生的创新和逆向思维能力.

练习册系列答案
相关题目
3.下列说法正确的是( )
| A. | 由同种元素组成的物质一定是单质 | |
| B. | 由不同种元素组成的物质一定是化合物 | |
| C. | 单质一定由同种元素组成 | |
| D. | 含氧化合物一定由两种元素组成 |
4.某气体可能含有H2、CO、CH4中的一种或两种.在空气中点燃该气体,用干燥玻璃片放在火焰上方,干燥玻璃片上有水雾,用另一个蘸有石灰水的烧杯罩在火焰上方,石灰水变浑浊.根据上述实验判断,该气体成分不可能是( )
| A. | CO、H2和CH4 | B. | H2和CO | C. | CH4 | D. | H2 |
8.用38%(密度为1.12g/cm3)的浓盐酸配制成200g19%的稀盐酸需加水( )
| A. | 50g | B. | 80g | C. | 100g | D. | 200g |
2.把铁片分别放入下列各物质的溶液中,片刻后取出,铁片质量减少的是( )
| A. | 硫酸铝 | B. | 硫酸铜 | C. | 硫酸 | D. | 硝酸银 |
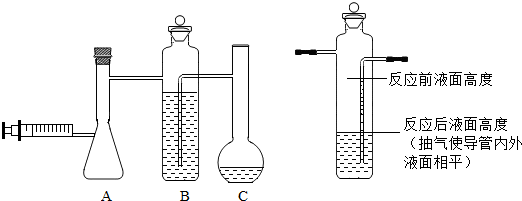
 如图所示,两个体积相等的集气瓶中充满了空气.如果右侧燃烧匙中是硫粉,硫粉燃烧后,待装置冷却至室温打开止水夹后,一开始观察右边集气瓶无变化;而烧杯中的水沿导管流入左边集气瓶中,直到集气瓶体积约$\frac{1}{5}$处;分析产生此现象的原因:因为硫在空气中燃烧,每消耗一分子氧气,就会生成一分子二氧化硫气体,使右边集气瓶中压强无变化;而磷在空气中燃烧,生成五氧化二磷固体,使得左边集气瓶中压强降低,大气将水压入瓶内直到气压平衡(即约占集气瓶体积的$\frac{1}{5}$处)..
如图所示,两个体积相等的集气瓶中充满了空气.如果右侧燃烧匙中是硫粉,硫粉燃烧后,待装置冷却至室温打开止水夹后,一开始观察右边集气瓶无变化;而烧杯中的水沿导管流入左边集气瓶中,直到集气瓶体积约$\frac{1}{5}$处;分析产生此现象的原因:因为硫在空气中燃烧,每消耗一分子氧气,就会生成一分子二氧化硫气体,使右边集气瓶中压强无变化;而磷在空气中燃烧,生成五氧化二磷固体,使得左边集气瓶中压强降低,大气将水压入瓶内直到气压平衡(即约占集气瓶体积的$\frac{1}{5}$处)..