题目内容
钢铁是使用最多的金属材料.(1)下图为实验室炼铁的装置图,A中反应的化学方程式是 ;将反应后的气体通过装置B和C,收集较纯净的CO并循环使用,B中应盛放的试剂是 浓溶液.
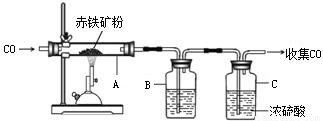
(2)工业上可用酸清洗锈蚀的金属.将生锈的铁片和生锈的铜片[铜锈的成分是Cu2(OH)2CO3]同时放入一定量盐酸中,可能发生的化学反应有:
①铜锈溶解:Cu2(OH)2CO3+4HCl=2CuCl2+3X+CO2↑,则X的化学式为 ;
②铁锈溶解:化学方程式为 ;
③有金属单质生成:化学方程式为 .
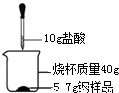
(3)某化学小组欲测定一种钢样品中铁的含量,实验操作如图所示,实验结果记录如下表:
| 反应时间 | t | t1 | t2 | t3 |
| 烧杯和药品质量/g | 55.7 | 55.6 | 55.5 | 55.5 |
②有同学提出,灼烧可使钢中的碳转化为二氧化碳,钢样品质量会减轻.但是他们将一定量的钢样品灼烧后,发现质量反而增加了,其原因是 .
【答案】分析:(1)根据一氧化碳可把三氧化二铁还原为铁写出化学反应式;收集较纯净的一氧化碳,需除去一氧化碳中的二氧化碳和水蒸汽;
(2)利用质量守恒定律写出X的化学式;酸与金属氧化物反应,,铁与生成的氯化铜反应;
(3)表中的实验数据可判断第四次称量时已完全反应,利用质量守恒定律,可计算放出氢气的质量;根据反应的化学方程式,由产生氢气质量计算钢样中所含铁的质量,求得钢样品中铁的质量分数.
解答:解:(1)实验室炼铁,A中发生反应是,一氧化碳把三氧化二铁还原为铁,并生成二氧化碳气体,化学反应式是:
3CO+Fe2O3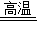 2Fe+3CO2;收集较纯净的一氧化碳要除去反应生成的二氧化碳和水蒸气,把气体通入盛放氢氧化钠溶液的试剂瓶,除去二氧化碳,再通入浓硫酸干燥气体;
2Fe+3CO2;收集较纯净的一氧化碳要除去反应生成的二氧化碳和水蒸气,把气体通入盛放氢氧化钠溶液的试剂瓶,除去二氧化碳,再通入浓硫酸干燥气体;
(2)将生锈的铁片和生锈的铜片[铜锈的成分是Cu2(OH)2CO3]同时放入一定量盐酸中,可能发生的化学反应,
①根据质量守恒定律,反应前后原子的个数和种类不变,得X的化学式为,H2O;
②铁锈与盐酸反应生成氯化铁和水,化学方程式为:Fe2O3+6HCl=2FeCl3+3H2O;
③铁置换出氯化铜中的铜,化学方程式为:CuCl2+Fe=Cu+FeCl2;
(3)①铁锈(Fe2O3)溶于盐酸(3)第四次称量时已完全反应,
根据质量守恒定律,反应中产生氢气的质量=40+5.7+10-55.5=0.2(g);
设样品中含铁的质量为xg.
Fe+2HCl=FeCl2+H2↑
56 2
x 0.2g
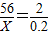 x=5.6g
x=5.6g
钢样品中铁的质量分数=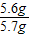 ×100%=98.2%
×100%=98.2%
②钢中含碳量少,灼烧时碳减少的质量,远小于铁转化为氧化物时增加的质量,所以将一定量的钢样品灼烧后,发现质量反而增加了.
故答案为:(1)3CO+Fe2O3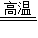 3CO2+2Fe,氢氧化钠(或NaOH);
3CO2+2Fe,氢氧化钠(或NaOH);
(2)H2O;Fe2O3+6HCl=2FeCl3+3H2O;CuCl2+Fe=Cu+FeCl2;
(3)98.2%;钢中含碳量少,所以碳减少的质量,远小于铁转化为氧化物时增加的质量.
点评:要熟记和理解一氧化碳还原氧化铁的所有内容,还有,铁等金属的冶炼原理、氧化还原反应的原理、一氧化碳的可燃性和毒性、金属的性质、化学方程式的书写、空气的污染等相关知识;然后,根据所给的实验、问题情景或图表信息等,结合所学的相关知识和技能,细致地阅读、分析题意等,联系着生活实际,细心地进行探究、推理,最后,按照题目的要求,认真地进行选择或解答即可.
(2)利用质量守恒定律写出X的化学式;酸与金属氧化物反应,,铁与生成的氯化铜反应;
(3)表中的实验数据可判断第四次称量时已完全反应,利用质量守恒定律,可计算放出氢气的质量;根据反应的化学方程式,由产生氢气质量计算钢样中所含铁的质量,求得钢样品中铁的质量分数.
解答:解:(1)实验室炼铁,A中发生反应是,一氧化碳把三氧化二铁还原为铁,并生成二氧化碳气体,化学反应式是:
3CO+Fe2O3
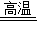 2Fe+3CO2;收集较纯净的一氧化碳要除去反应生成的二氧化碳和水蒸气,把气体通入盛放氢氧化钠溶液的试剂瓶,除去二氧化碳,再通入浓硫酸干燥气体;
2Fe+3CO2;收集较纯净的一氧化碳要除去反应生成的二氧化碳和水蒸气,把气体通入盛放氢氧化钠溶液的试剂瓶,除去二氧化碳,再通入浓硫酸干燥气体;(2)将生锈的铁片和生锈的铜片[铜锈的成分是Cu2(OH)2CO3]同时放入一定量盐酸中,可能发生的化学反应,
①根据质量守恒定律,反应前后原子的个数和种类不变,得X的化学式为,H2O;
②铁锈与盐酸反应生成氯化铁和水,化学方程式为:Fe2O3+6HCl=2FeCl3+3H2O;
③铁置换出氯化铜中的铜,化学方程式为:CuCl2+Fe=Cu+FeCl2;
(3)①铁锈(Fe2O3)溶于盐酸(3)第四次称量时已完全反应,
根据质量守恒定律,反应中产生氢气的质量=40+5.7+10-55.5=0.2(g);
设样品中含铁的质量为xg.
Fe+2HCl=FeCl2+H2↑
56 2
x 0.2g
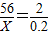 x=5.6g
x=5.6g钢样品中铁的质量分数=
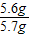 ×100%=98.2%
×100%=98.2%②钢中含碳量少,灼烧时碳减少的质量,远小于铁转化为氧化物时增加的质量,所以将一定量的钢样品灼烧后,发现质量反而增加了.
故答案为:(1)3CO+Fe2O3
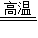 3CO2+2Fe,氢氧化钠(或NaOH);
3CO2+2Fe,氢氧化钠(或NaOH);(2)H2O;Fe2O3+6HCl=2FeCl3+3H2O;CuCl2+Fe=Cu+FeCl2;
(3)98.2%;钢中含碳量少,所以碳减少的质量,远小于铁转化为氧化物时增加的质量.
点评:要熟记和理解一氧化碳还原氧化铁的所有内容,还有,铁等金属的冶炼原理、氧化还原反应的原理、一氧化碳的可燃性和毒性、金属的性质、化学方程式的书写、空气的污染等相关知识;然后,根据所给的实验、问题情景或图表信息等,结合所学的相关知识和技能,细致地阅读、分析题意等,联系着生活实际,细心地进行探究、推理,最后,按照题目的要求,认真地进行选择或解答即可.

练习册系列答案
相关题目

 钢铁是使用最多的金属材料.
钢铁是使用最多的金属材料.
