题目内容
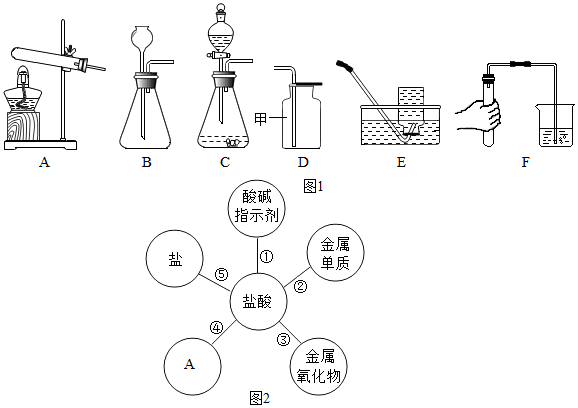
14.某化学兴趣小组同学对实验室里的粗盐样品进行了如下实验探究:
(1)操作②的名称是过滤,实验中多次用到玻璃棒,操作③中玻璃棒的作用是防止局部过热造成液滴飞溅.
(2)用提纯得到的“精盐”配制100g10%的氯化钠溶液,经检测,溶质质量分数偏小,其原因可能有①②③(填序号).
①精盐不干燥 ②称量时精盐与砝码放反了
③量取水时仰视读数 ④装瓶时,有少量溶液洒出
(3)查阅资料得知:粗盐中除含少量泥沙等不溶性杂质外,还含有少量的可溶性杂质(假定可溶性杂质只有MgCl2一种)为了得到较纯净的氯化钠,小组同学将所得的“精盐”又做了如下处理:
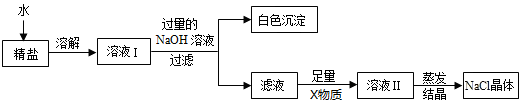
①实验中加入过量的氢氧化钠溶液,发生反应的化学方程式为MgCl2+2NaOH=Mg(OH)2↓+2NaCl.
②在得到的滤液中加入足量的X物质,该物质的化学式为HCl.
③若实验过程中不考虑损耗,最终到的NaCl固体的质量将大于(填“大于”、“小于”或“等于”)原精盐中NaCl的质量.
分析 (1)根据过滤可以将不溶物和可溶物分离,以及玻璃棒在搅拌过程中的作用进行分析;
(2)根据氯化钠溶液的质量分数偏小,可能是氯化钠质量少了,也可能是水的质量多了进行分析;
(3)①根据氢氧化钠和氯化镁会生成氢氧化镁沉淀进行分析;
②根据除去氯化镁加入的氢氧化钠是过量的,对于氯化钠也是杂质进行分析;
③根据氢氧化钠和氯化镁会生成氯化钠,盐酸和氢氧化钠也会生成氯化钠进行分析.
解答 解:(1)过滤可以将不溶物和可溶物分离,所以操作③的名称是过滤,操作④是蒸发,要用到玻璃棒,作用为防止局部过热造成液滴飞溅;
(2)氯化钠溶液的质量分数偏小,可能是氯化钠质量少了,也可能是水的质量多了;
①氯化钠固体不干燥,会导致氯化钠质量偏小,溶质质量分数偏小,故①正确;
②称量时精盐与砝码放反了,氯化钠质量等于砝码质量-游码质量,会导致氯化钠质量偏小,溶质质量分数偏小,故②正确;
③量取水时仰视读数,导致水的体积偏大,溶质质量分数偏小,故③正确;
④装瓶时,有少量溶液洒出,质量分数不变,故④错误.
故选:①②③;
(3)①氢氧化钠和氯化镁会生成氢氧化镁沉淀和氯化钠,化学方程式为:MgCl2+2NaOH=Mg(OH)2↓+2NaCl;
②除去氯化镁加入的氢氧化钠是过量的,对于氯化钠也是杂质,所以在得到的滤液中加入足量的稀盐酸;
③氢氧化钠和氯化镁会生成氯化钠,盐酸和氢氧化钠也会生成氯化钠,所以实验过程中不考虑损耗,最终到的NaCl固体的质量将大于原精盐中NaCl的质量.
故答案为:(1)过滤,防止局部过热造成液滴飞溅;
(2)①②③;
(3)①MgCl2+2NaOH=Mg(OH)2↓+2NaCl;
②HCl;
③大于.
点评 本题主要考查了粗盐提纯的相关知识,难度不大,需要在平时多加记忆.

练习册系列答案
 新课标快乐提优暑假作业陕西旅游出版社系列答案
新课标快乐提优暑假作业陕西旅游出版社系列答案
相关题目
9.下列实验中,水起隔绝氧气作用的是( )
| A. | 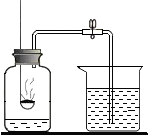 测空气中氧气含量 | B. | 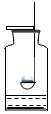 硫在氧气中燃烧 | ||
| C. |  燃烧条件的实验 | D. |  试管的洗涤 |
5.海洋是一个巨大的宝藏,期待着人们的开发和利用.下列物质不经过化学变化就能从海水中获得的是( )
| A. | 纯碱 | B. | 单质镁 | C. | 烧碱 | D. | 粗盐 |
19.将m 克10%的NaOH溶液与m 克10%的硫酸溶液混合后,再滴入紫色石蕊试液,溶液显( )
| A. | 紫色 | B. | 红色 | C. | 蓝色 | D. | 无色 |
4.某元素R的化合价是偶数(不变价),其氯化物的相对分子质量是m,其氧化物的相对分子质量是n,则R的化合价是( )
| A. | $\frac{2(m-n)}{55}$ | B. | $\frac{2(n-m)}{55}$ | C. | $\frac{2m-n}{55}$ | D. | $\frac{2n-m}{55}$ |