题目内容
(2011?白下区二模)铁矿石冶炼成铁是一个复杂的过程,把铁矿石和焦炭、石灰石一起加入高炉,在高温下,利用焦炭与氧气反应生成的一氧化碳把铁从铁矿石里还原出来.一氧化碳还原氧化铁的化学方程式为______ 2Fe+3CO2
【答案】分析:熟记一氧化碳还原氧化铁的化学反应式;
【提出问题】熟记碳还原氧化铁的化学反应式;
【进行实验】②根据可燃性气体与空气混合加热时有爆炸的危险考虑;
【实验现象】根据氧化铁是红色,铁粉是黑色分析判断现象;
【交流与反思】根据实验完成后还要考虑分离出所要得到的物质考虑;
【完善实验】根据澄清石灰水可以检验二氧化碳、氢氧化钠溶液可以吸收二氧化碳、一氧化碳可以还原氧化铜并生成二氧化碳气体考虑;
【拓展延伸】(1)认真分析其原理,利用大气压强的知识来解释检验装置气密性的方法;
(2)为使测得的气体体积更精确,记录c中液面刻度时,除使视线与凹液面的最低处相平外,还应d处观察上升的是否与c中下降的一致;以尽量减少误差;
(3)如果实验过程中,发现稀硫酸的量不足,应中途加酸还是重新实验:中途添加酸时,会造成气体逸散,影响气体体积的精确测量
(4)已知气体的体积,根据密度,可以求出气体的质量;但不知道剩余固体质量或铁粉的质量,无法计算.所以实验中由于缺少某一步骤导致数据缺乏而无法计算,该步骤是:测量装置B反应后所得的固体质量(或测量铁粉的质量).
解答:解:一氧化碳还原氧化铁的化学反应式是:3CO+Fe2O3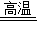 2Fe+3CO2.
2Fe+3CO2.
故答案为:3CO+Fe2O3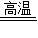 2Fe+3CO2;
2Fe+3CO2;
【提出问题】碳还原氧化铁的化学反应式是:3C+2Fe2O3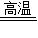 4Fe+3CO2↑.
4Fe+3CO2↑.
故答案为:3C+2Fe2O3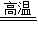 4Fe+3CO2↑;
4Fe+3CO2↑;
【进行实验】为防止一氧化碳与空气混合加热时,引起爆炸,在实验前要先通入CO;防止高温下铁又被进入的空气氧化,实验结束后,应继续通入CO直至冷却至室温.
故答案为:通入CO;防止高温下铁又被进入的空气氧化;
【实验现象】因氧化铁是红色,铁粉是黑色,B中的氧化铁被完全还原后,由红色变成黑色.此时由于A中的氧化铁还没有被完全还原,仍有红色物质.
故答案为:红色变为黑色;红色物质;
【交流与反思】实验完成后还要考虑分离出所要得到的铁,焦炭和铁都是固体,不易分离,也是不用碳还原氧化铁的原因.
故答案为:焦炭是固体,不容易和生成的铁分离(合理即可)
【完善实验】澄清石灰水可以检验二氧化碳、氢氧化钠溶液可以吸收二氧化碳、一氧化碳可以还原氧化铜并生成二氧化碳气体,所以先用C检验二氧化碳的存在,为防止二氧化碳影响实验的结论,再用D中的氢氧化钠溶液吸收二氧化碳,再次连接C检查二氧化碳是否被完全吸收;然后将气体通过E,并再次连接C,如果氧化铜由黑色变成红色,C中的澄清石灰水变浑浊,说明有一氧化碳气体.因有一氧化碳存在,要进行尾气处理,而图中缺少此装置.
故答案为:C→D→C→E→C;缺少尾气处理装置;
【拓展延伸】(1)注意检验该装置的气密性的方法:提高d管,静止片刻后,c、d液面仍存在高度差,则气密性良好.
故答案为:提高d管,静止片刻后,c、d液面仍存在高度差,则气密性良好;
(2)除使视线与凹液面的最低处相平外,还应d处观察上升的是否与c中下降的一致.
故答案为:使d、c中的液面相平;
(3)中途添加酸时,会造成气体逸散,影响气体体积的精确测量,所以要重新实验.
故答案为:重新实验;
(4)已知气体的体积,根据密度,可以求出气体的质量,但不知道装置B反应后所得的固体质量(或测量铁粉的质量),无法计算.实验中由于数据缺乏而无法计算,该步骤是:装置B反应后所得的固体质量(或测量铁粉的质量).
故答案为:测量装置B反应后所得的固体质量(或测量铁粉的质量).
点评:本题以实验探究的形式考查化学反应式的书写、实验中的注意事项、以及不用碳还原氧化铁的原因,还有相关的拓展实验,可谓考查详尽,即考查了知识,又培养了学生的细心、耐心分析解决问题的能力.
【提出问题】熟记碳还原氧化铁的化学反应式;
【进行实验】②根据可燃性气体与空气混合加热时有爆炸的危险考虑;
【实验现象】根据氧化铁是红色,铁粉是黑色分析判断现象;
【交流与反思】根据实验完成后还要考虑分离出所要得到的物质考虑;
【完善实验】根据澄清石灰水可以检验二氧化碳、氢氧化钠溶液可以吸收二氧化碳、一氧化碳可以还原氧化铜并生成二氧化碳气体考虑;
【拓展延伸】(1)认真分析其原理,利用大气压强的知识来解释检验装置气密性的方法;
(2)为使测得的气体体积更精确,记录c中液面刻度时,除使视线与凹液面的最低处相平外,还应d处观察上升的是否与c中下降的一致;以尽量减少误差;
(3)如果实验过程中,发现稀硫酸的量不足,应中途加酸还是重新实验:中途添加酸时,会造成气体逸散,影响气体体积的精确测量
(4)已知气体的体积,根据密度,可以求出气体的质量;但不知道剩余固体质量或铁粉的质量,无法计算.所以实验中由于缺少某一步骤导致数据缺乏而无法计算,该步骤是:测量装置B反应后所得的固体质量(或测量铁粉的质量).
解答:解:一氧化碳还原氧化铁的化学反应式是:3CO+Fe2O3
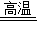 2Fe+3CO2.
2Fe+3CO2.故答案为:3CO+Fe2O3
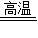 2Fe+3CO2;
2Fe+3CO2;【提出问题】碳还原氧化铁的化学反应式是:3C+2Fe2O3
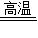 4Fe+3CO2↑.
4Fe+3CO2↑.故答案为:3C+2Fe2O3
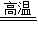 4Fe+3CO2↑;
4Fe+3CO2↑;【进行实验】为防止一氧化碳与空气混合加热时,引起爆炸,在实验前要先通入CO;防止高温下铁又被进入的空气氧化,实验结束后,应继续通入CO直至冷却至室温.
故答案为:通入CO;防止高温下铁又被进入的空气氧化;
【实验现象】因氧化铁是红色,铁粉是黑色,B中的氧化铁被完全还原后,由红色变成黑色.此时由于A中的氧化铁还没有被完全还原,仍有红色物质.
故答案为:红色变为黑色;红色物质;
【交流与反思】实验完成后还要考虑分离出所要得到的铁,焦炭和铁都是固体,不易分离,也是不用碳还原氧化铁的原因.
故答案为:焦炭是固体,不容易和生成的铁分离(合理即可)
【完善实验】澄清石灰水可以检验二氧化碳、氢氧化钠溶液可以吸收二氧化碳、一氧化碳可以还原氧化铜并生成二氧化碳气体,所以先用C检验二氧化碳的存在,为防止二氧化碳影响实验的结论,再用D中的氢氧化钠溶液吸收二氧化碳,再次连接C检查二氧化碳是否被完全吸收;然后将气体通过E,并再次连接C,如果氧化铜由黑色变成红色,C中的澄清石灰水变浑浊,说明有一氧化碳气体.因有一氧化碳存在,要进行尾气处理,而图中缺少此装置.
故答案为:C→D→C→E→C;缺少尾气处理装置;
【拓展延伸】(1)注意检验该装置的气密性的方法:提高d管,静止片刻后,c、d液面仍存在高度差,则气密性良好.
故答案为:提高d管,静止片刻后,c、d液面仍存在高度差,则气密性良好;
(2)除使视线与凹液面的最低处相平外,还应d处观察上升的是否与c中下降的一致.
故答案为:使d、c中的液面相平;
(3)中途添加酸时,会造成气体逸散,影响气体体积的精确测量,所以要重新实验.
故答案为:重新实验;
(4)已知气体的体积,根据密度,可以求出气体的质量,但不知道装置B反应后所得的固体质量(或测量铁粉的质量),无法计算.实验中由于数据缺乏而无法计算,该步骤是:装置B反应后所得的固体质量(或测量铁粉的质量).
故答案为:测量装置B反应后所得的固体质量(或测量铁粉的质量).
点评:本题以实验探究的形式考查化学反应式的书写、实验中的注意事项、以及不用碳还原氧化铁的原因,还有相关的拓展实验,可谓考查详尽,即考查了知识,又培养了学生的细心、耐心分析解决问题的能力.

练习册系列答案
相关题目



