题目内容
如图是实验室所用盐酸的试剂瓶上标签的部分内容.请仔细阅读后计算:(1)欲配制14.3%的稀盐酸200g,需要用这种盐酸多少毫升?
(2)13g锌与足量的稀盐酸充分反应,理论上可制得氢气多少克?
(3)需要用这种盐酸的质量是多少?

【答案】分析:(1)本小题属于溶液稀释问题,配制过程中溶质质量不变,据此可以计算出所需盐酸的质量,再结合密度可以计算出其体积.
(2)由锌的质量根据锌与盐酸反应的化学方程式可以计算出生成氢气的质量.
(3)由锌的质量根据锌与盐酸反应的化学方程式可以计算出需要的盐酸的质量.
解答:解:(1)需用盐酸的体积为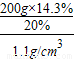 =130cm3=130mL
=130cm3=130mL
(2)设生成氢气的质量是x,需要这种盐酸的质量是y.
Zn+2HCl=ZnCl2+H2↑
65 73 2
13g y×20% x
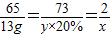
x=0.4g y=73g
(3)由(2)的计算可知需要这种盐酸的质量是73g;
答:(1)需要这种盐酸130mL.(2)理论上可制得氢气0.4g.(3)需要用这种盐酸的质量是73g;
点评:本题考查了溶质质量分数以及根据化学方程式的有关计算,完成此题,可以依据溶质质量分数公式以及化学方程式计算.
(2)由锌的质量根据锌与盐酸反应的化学方程式可以计算出生成氢气的质量.
(3)由锌的质量根据锌与盐酸反应的化学方程式可以计算出需要的盐酸的质量.
解答:解:(1)需用盐酸的体积为
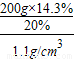 =130cm3=130mL
=130cm3=130mL(2)设生成氢气的质量是x,需要这种盐酸的质量是y.
Zn+2HCl=ZnCl2+H2↑
65 73 2
13g y×20% x
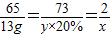
x=0.4g y=73g
(3)由(2)的计算可知需要这种盐酸的质量是73g;
答:(1)需要这种盐酸130mL.(2)理论上可制得氢气0.4g.(3)需要用这种盐酸的质量是73g;
点评:本题考查了溶质质量分数以及根据化学方程式的有关计算,完成此题,可以依据溶质质量分数公式以及化学方程式计算.

练习册系列答案
相关题目
 如图是实验室所用盐酸试剂瓶上标签的部分内容,请仔细阅读后计算:
如图是实验室所用盐酸试剂瓶上标签的部分内容,请仔细阅读后计算: 如图是实验室所用盐酸试剂瓶上标签的部分内容,、请仔细阅读后计算:
如图是实验室所用盐酸试剂瓶上标签的部分内容,、请仔细阅读后计算: 如图是实验室所用盐酸试剂瓶上标签的部分内容,请仔细阅读后计算:
如图是实验室所用盐酸试剂瓶上标签的部分内容,请仔细阅读后计算:
