题目内容
下图是小梅配制100g溶质质量分数为12%的NaCl溶液的实验操作示意图:

(1)计算:需要NaCl的质量为 g,需要水的体积为 mL.
(2)上图中的玻璃仪器分别是广口瓶、量筒、 、 .
(3)指出图中的一处错误操作 .
(4)配制时应选择 mL(10mL或50mL或100mL)的量筒量取所需要的水.用上述图示的序号表示配制溶液的操作顺序 .

(1)计算:需要NaCl的质量为
(2)上图中的玻璃仪器分别是广口瓶、量筒、
(3)指出图中的一处错误操作
(4)配制时应选择
考点:一定溶质质量分数的溶液的配制,测量容器-量筒
专题:溶液、浊液与溶解度
分析:(1)根据溶质质量分数的计算公式计算;
(2)根据配制溶液所需的仪器考虑本题;
(3)根据配制溶液的操作过程中的注意事项考虑;
(4)溶质质量=溶液质量×溶质质量分数,溶剂质量=溶液质量-溶质质量然后根据量筒的规格选择量筒,最后根据配制溶液的基本步骤解答.
(2)根据配制溶液所需的仪器考虑本题;
(3)根据配制溶液的操作过程中的注意事项考虑;
(4)溶质质量=溶液质量×溶质质量分数,溶剂质量=溶液质量-溶质质量然后根据量筒的规格选择量筒,最后根据配制溶液的基本步骤解答.
解答:解:(1)氯化钠质量:100g×12%=12g,需水:100g-12g=88g合88mL水;故答案:12;88;
(2)配制溶液需要广口瓶、烧杯、量筒和玻璃棒这四种玻璃仪器;故答案:烧杯、玻璃棒;
(3)用天平称量物质时要左物右码,而图示中却是左码右物;故答案:装置②中氯化钠与砝码的位置颠倒了;
(4)需要88mL的水,所以选用100mL的量筒;配制溶质质量分数一定的溶液的基本步骤:计算、称量、量取、溶解、装瓶存放,要注意在称量前先取出药品才能称量;故答案:100;④②①⑤③.
(2)配制溶液需要广口瓶、烧杯、量筒和玻璃棒这四种玻璃仪器;故答案:烧杯、玻璃棒;
(3)用天平称量物质时要左物右码,而图示中却是左码右物;故答案:装置②中氯化钠与砝码的位置颠倒了;
(4)需要88mL的水,所以选用100mL的量筒;配制溶质质量分数一定的溶液的基本步骤:计算、称量、量取、溶解、装瓶存放,要注意在称量前先取出药品才能称量;故答案:100;④②①⑤③.
点评:通过回答本题知道了溶质、溶剂质量的计算方法,用天平称量时的注意事项,掌握了配制溶质质量分数一定的溶液的基本步骤.

练习册系列答案
相关题目
把NaOH溶液和CuSO4溶液加入某病人的尿液中,微热,如果观察到红色沉淀,说明该尿液中含有( )
| A、食醋 | B、白酒 | C、葡萄糖 | D、食盐 |



 实验室利用如图1所示装置进行加热氯酸钾制氧气的实验.
实验室利用如图1所示装置进行加热氯酸钾制氧气的实验.
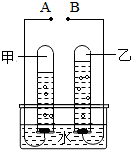 如图是电解水的实验装置图,请根据你所了解的知识填空
如图是电解水的实验装置图,请根据你所了解的知识填空