题目内容
氯酸钾和二氧化锰的混合物共14克,加热至不现产生气体为止,称得剩余固体质量为9.2克,求剩余固体的组成.(Cl:35.5;K:39 Mn:55)
考点:根据化学反应方程式的计算
专题:有关化学方程式的计算
分析:反应前后的质量差即为反应生成氧气的质量,根据氧气的质量可以计算氯化钾的质量和氯酸钾的质量,进一步可以计算二氧化锰的质量.
解答:解:剩余固体为氯化钾和二氧化锰的混合物,
生成氧气的质量为:14g-9.2g=4.8g,
设氯酸钾的质量为x,生成氯化钾的质量为y
2KClO3
2KCl+3O2↑,
245 149 96
x y 4.8g
=
=
x=12.25g,y=7.45g
原混合物中二氧化锰的质量为:14g-12.25g=1.75g
答:剩余固体中氯化钾的质量为7.45g,二氧化锰的质量为1.75g.
生成氧气的质量为:14g-9.2g=4.8g,
设氯酸钾的质量为x,生成氯化钾的质量为y
2KClO3
| ||
| △ |
245 149 96
x y 4.8g
| 245 |
| x |
| 149 |
| y |
| 96 |
| 4.8g |
x=12.25g,y=7.45g
原混合物中二氧化锰的质量为:14g-12.25g=1.75g
答:剩余固体中氯化钾的质量为7.45g,二氧化锰的质量为1.75g.
点评:本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列关于实验现象的描述,正确的是( )
| A、在试管中加入5mL5%的过氧化氢溶液,将带火星的木条伸入试管,木条复燃 |
| B、向盛有水的小烧杯中加入少量品红,一段时间,烧杯内的液体变为红色 |
| C、木炭在氧气中燃烧产生白色火焰 |
| D、石灰石和足量稀盐酸反应时,固体表面有大量的二氧化碳气体产生 |
关于O2、CO2、SO2、H2O2四种物质,下列叙述正确的是( )
| A、都有氧分子 |
| B、一个分子中都含有两个氧原子 |
| C、都是氧化物 |
| D、都是化合物 |
 向盛有22.3g Na2CO3和NaCl固体混合物的烧杯中加入216.1g稀盐酸恰好反应,反应过程用精密仪器测得烧杯连同药品的质量(m)与反应时间(t)的关系如图所示:烧杯连同药品的起始质量为300g.回答下列问题:
向盛有22.3g Na2CO3和NaCl固体混合物的烧杯中加入216.1g稀盐酸恰好反应,反应过程用精密仪器测得烧杯连同药品的质量(m)与反应时间(t)的关系如图所示:烧杯连同药品的起始质量为300g.回答下列问题:
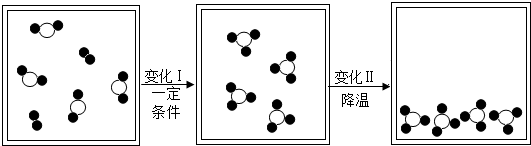
 代表硫原子)
代表硫原子)