题目内容
8.下列固体物质加入到盛有一定量水的烧杯中,能使水温度升高的是( )| A. | 硝酸铵 | B. | 硫酸铜 | C. | 生石灰 | D. | 氯化钾 |
分析 根据物质溶于水后的放热与吸热现象来考虑,要由物质溶于水的整个过程来分析,到底是吸收的热量大于放出的热量,还是吸收的热量小于放出的热量.
解答 解:物质溶于水分为两个过程,向水中扩散的过程吸收热量,与水分子结合形成水合分子的过程放出热量,如果吸收热量大于放出热量,就表现为吸热,如果吸收热量小于放出热量,就表现为放热,如果相等就表现为既不放热,也不吸热.
A、硝酸铵溶于水吸收热量,故A错;
B、硫酸铜溶于水溶液温度基本不变,故B错误.
C、生石灰溶于水放出热量,溶液温度升高,故C正确;
D、氯化钾溶于水溶液温度基本不变,故D错.
故选C
点评 熟记以下物质:溶于水放热的物质有:浓硫酸、生石灰、氢氧化钠固体;溶于水吸热的有硝酸铵.

练习册系列答案
 名牌中学课时作业系列答案
名牌中学课时作业系列答案 明天教育课时特训系列答案
明天教育课时特训系列答案 浙江新课程三维目标测评课时特训系列答案
浙江新课程三维目标测评课时特训系列答案 周周清检测系列答案
周周清检测系列答案
相关题目
13.将20gCaCO3隔绝空气高温煅烧一段时间后停止,剩余固体中钙元素的质量分数为50%,则整个过程中产生二氧化碳的质量为( )
| A. | 2.2g | B. | 4g | C. | 4.4g | D. | 8g |
13.如图所示为甲、乙两种固体的溶解度曲线,下列说法正确的是( )
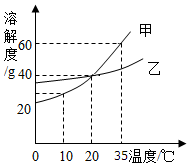

| A. | 10℃时,甲的溶解度小于乙的溶解度 | |
| B. | 甲的溶解度大于乙的溶解度 | |
| C. | 20℃时,把30g甲放入50g水中形成的溶液中溶质与溶剂的质量比为3:5 | |
| D. | 等质量的甲、乙饱和溶液,从35℃降温至10℃时,二者溶质质量分数相等 |
17.下列关于化学变化的说法,不正确的是( )
| A. | 分子一定发生变化 | B. | 原子核一定不发生变化 | ||
| C. | 元素的种类可能发生变化 | D. | 元素的化合价不一定发生变化 |


